微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 用中和滴定法确定某烧碱样品的浓度,试根据实验回答下列问题:
(1)准确称取一定量的样品,配成500 mL待测溶液。称量时,样品可放在 (填编号字母)上称量
(A)小烧杯????(B)洁净纸片??(C)直接放在托盘上
(2)准确量取10.00ml待测液于锥形瓶中,用0.2000mol・L-1的盐酸来滴定待测溶液,不可选用??????(填编号字母)作指示剂。 (A)甲基橙??(B)石蕊??(C)酚酞???
(3)若选用甲基橙作指示剂,滴定终点的判断依据是????????????????????????????
???????????????????????此时溶液显????????性。
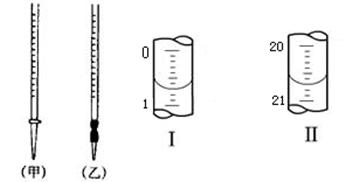
(4)0.2000mol・L-1的盐酸应装在下图所示的??????????(填甲、乙)中,图Ⅰ所示为滴定前液面,图Ⅱ所示为滴定结束时液面,根据图示计算被测烧碱溶液的物质的量浓度是??????????????mol・L-1。
(5)下列实验操作会对滴定结果产生的后果。(填“偏高”、“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果???????????。
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果?????????。
2、选择题 为中和物质的量为amol的某酸bg,需物质的量浓度为cmol/L的碱溶液的体积为
3、选择题 能表示人大量喝水时胃液的pH变化的图象是(??? )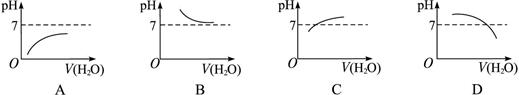
4、选择题 下列热化学方程式书写正确的是(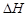 的绝对值均正确)
的绝对值均正确)
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)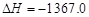 kJ/mol(燃烧热)
kJ/mol(燃烧热)
B.NaOH(aq)+HCl (aq)===NaCl (aq) +H2O(l)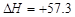 kJ/mol(中和热)
kJ/mol(中和热)
C.S(s)+O2(g)===SO2(g)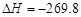 kJ/mol(反应热)
kJ/mol(反应热)
D.Fe+S===FeS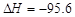 kJ/mol(反应热)
kJ/mol(反应热)
5、选择题 下列说法正确的是
A.已知 则可以计算CH3―CH3 → CH2=CH2+H2;ΔH =+125.6 kJ/mol
则可以计算CH3―CH3 → CH2=CH2+H2;ΔH =+125.6 kJ/mol
B.能说明NH3结合H+能力比H2O强:NH3+H3O+=NH+4+H2O
C.已知下列热化学方程式:2H2(g)+O2(g) ="==" 2H2O(g) △H=-484kJ/mol,则氢气的燃烧热为-242kJ/mol
D.已知中和热为-57.4kJ/mol ,则NaOH(aq) +CH3COOH(aq)=CH3COONa(aq)+H2O(l);△H =-57.4kJ/mol