微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是(??)

参考答案:C
本题解析:反应分为两个阶段:(1)Al(NO3)3+3NaOH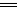 Al(OH)3↓+3NaNO3,
Al(OH)3↓+3NaNO3,
Mg(NO3)2+2NaOH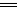 本题难度:简单
本题难度:简单
2、选择题 下表中各组物质不能实现如图转化的是
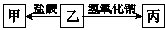
?
| 甲
| 乙
| 丙
|
A
| AlCl3
| Al
| Al(OH)3
|
B
| AlCl3
| Al(OH)3
| NaAlO2
|
C
| CO2
| NaHCO3
| Na2CO3
|
D
| CO2
| (NH4)2CO3
| NH3
参考答案:A
本题解析:
试题分析:A中铝和氢氧化钠反应只能生成偏铝酸钠。故选A。
点评:历年高考对铝的考查都不少,所以对考生的要求就是熟练掌握和铝相关的各种转化关系,以及氯化铝和氢氧化钠的相互滴加,偏铝酸钠和盐酸的相互滴加等试验。
本题难度:简单
3、选择题 下列有关厨房中铝制品使用合理的是[???? ]
A.盛放食醋
B.烧煮开水
C.用碱水洗涤
D.用金属丝擦洗表面的污垢
参考答案:B
本题解析:
本题难度:简单
4、选择题 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。

则原溶液中Al3+、Mg2+、NH4+的物质的量分别为 ( ?)
A.2 mol、3 mol、8 mol
B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol
D.3 mol、2 mol、4 mol
参考答案:C
本题解析:
加入8molNa2O2时,根据钠原子守恒,可知n(Na+)=2n(Na2O2)=2×8mol=16mol,Na+离子所带的总电量相当于16mol×1=16mol.
A、Al3+、Mg2+、NH4+离子所带的总电量相当于2mol×3+3mol×2+8mol×1=20mol,故A错误;
B、Al3+、Mg2+、NH4+离子所带的总电量相当于3mol×3+2mol×2+8mol×1=21mol,故B错误;
C、Al3+、Mg2+、NH4+离子所带的总电量相当于2mol×3+3mol×2
本题难度:困难
5、选择题 铝分别与足量的稀硫酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的硫酸和NaOH物质的量之比为
A.1:1
B.3:1
C.3:2
D.1:3
参考答案:C
本题解析:
试题分析:反应的有关方程式为:铝与盐酸:2Al+6HCl=2AlCl3+3H2↑,铝与NaOH溶液:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;假设生成的氢气的物质的量为3mol,根据方程式计算NaOH、HCl的物质的量,从而计算出氢氧化钠和氯化氢物质的量的之比。设生成的氢气的物质的量为3mol,则:
2Al+6HCl=2AlCl3+3H2↑
6mol??????3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2mol?????????3mol
本题难度:一般
|