微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 实验室有NH4HCO3和NaHSO3的干燥粉状混合物,某兴趣小组为测定其中NH4HCO3的含量,设计了用在混合物中加酸的实验方法来测定其质量分数。化学小组主要选用了下列药品和仪器进行实验(铁架台等固定仪器未画出)。按气流由左向右的方向,仪器连接顺序是 。回答以下问题:
。回答以下问题:

(1)A中加入硫酸溶液的仪器名称是:???????????????????。
(2)实验开始,混合物加酸前,A装置需要鼓入空气,排除装置中原有的空气。加酸后A装置再次鼓入空气的作用是???????????? ???????。
(3)E装置的作用是???????????????????????????????????? ?????????????????。
(4)实验中,要确保实验中C瓶溶液不褪色,若C瓶中溶液褪色,则测定结果可能会偏??? ??(填“高”或“低”)。
(5)若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质量分数为?????????? ???。
(6)从定量测定的准确性考虑,该套装置还应作进一步的改进是????????????????????。
参考答案:(12分)(1)分液漏斗(2分)
(2)将生成的气体全
本题解析:
试题分析:(1)根据仪器的构造特点可知,A中加入硫酸溶液的仪器名称是分液漏斗。
(2)加酸后生成CO2和SO2气体,所以加酸后A装置再次鼓入空气的作用是将生成的气体全部送入后续装置(使反应产生的SO2和CO2被完全吸收)。
(3)由于SO2也能碱石灰吸收,会干扰CO2的测定,所以高锰酸钾溶液的作用是除去SO2,以防止SO2对测定结果的影响。
(4)若C瓶中溶液褪色,说明SO没有完全被除尽,也被碱石灰吸收,则测定结果可能会偏高。
(5)碱石灰增重4.4g,则反应中生成的CO2的质量就是4.4g,物质的量是0.1mol。则根据碳原子守恒可知,碳酸氢铵的物质的量也是0.1mol,质量是7.9g,所以混合物中NH4HCO3的质量分数为 。
。
(6)由于空气中也含有水蒸气和CO2,也能被碱石灰吸收,所以从定量测定的准确性考虑,该套装置还应作进一步的改进是在B之后再接一个阻止空气中水蒸气和二氧化碳进入B的装置。
点评:该题是高考中的常见题型,属于中等难度的试题,试题综合性强,难易适中,在注重对学生基础知识检验与巩固的同时,侧重对学生能力的培养和实验能力的训练与指导。有助于培养学生规范、严谨的实验设计能力,提高学生的综合实验能力,提升学生的学科素养。该类试题重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般
2、简答题 Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题:
(1)甲同学取一束细铜丝用砂纸打磨后在酒精灯上加热至红热,再伸到Cl2的集气瓶中.你认为甲同学在实验中应该观察到的现象是______.
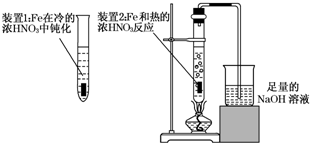
(2)乙同学为验证Fe在冷的浓HNO3中发生钝化但能和热的浓HNO3反应,设计了如图所示的实验,请你指出其中的两处错误:______、______;纠正上述错误后,请你从绿色化学的角度出发,对装置2提出改进建议,使装置2既能控制反应的进行,又能减少氮氧化物的排放:______.
(3)丙同学在Fe和浓HNO3反应后的溶液中加入一块Cu片,Cu片逐渐溶解,反应一段时间后不再溶解(Cu有剩余).
①丙同学依据反应现象得出Cu片溶解的原因是和HNO3发生反应.他依据的反应现象是______.
②丁同学认为丙同学的结论不完全正确.他的理由是______.
(4)请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+.说明具体的操作和实验现象______.
参考答案:(1)铜在氧气中不燃烧,在氯气中能燃烧产生棕黄色烟,故答案为
本题解析:
本题难度:一般
3、填空题 (12分)甲、乙两人分别用不同的方法配制100mL 3.6mol/L的稀硫酸。
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为??????????????????????????????
(2)甲:量取18 mol/L的浓硫酸?????????????mL,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小 心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①实验所用的玻璃仪器除烧杯和容量瓶外,还有?????????、????????、??????????;
②使用容量瓶前必须进行的一步操作是???????????????????
③ 定容的正确操作是????????????????????????????????????????????????
(3)乙:用100 mL量筒量取20 mL浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加水至100 mL 刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中 错误之处???????????????????????????
错误之处???????????????????????????
参考答案:(12分)(1)②①③⑧⑤⑥⑦④ (2分,错排不得分)
本题解析:略
本题难度:一般
4、简答题 如图是实验室制SO2并验证SO2某些性质的装置图.
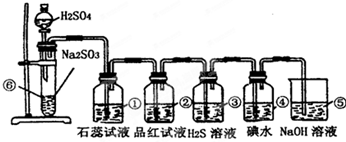
试回答:
(1)①中的实验现象是______,此实验证明SO2是______性气体.
(2)②中的品红溶液______,证明SO2有______性.
(3)③中的实验现象是______,证明SO2有______性.化学反应方程式______
(4)④中的实验现象是______,证明SO2有______性.化学反应方程式______
(5)⑤中的作用是______,反应的化学方程式是______.
参考答案:(1)①二氧化硫与水反应生成亚硫酸,遇石蕊变红,则实验现象变
本题解析:
本题难度:一般
5、填空题 以黄铜矿(CuFeS2)为原料冶炼铜的反应为:
8CuFeS2+21O2
(1)若Cu为+2价,则反应中每生成1molCu需要转移?????????????mol电子。
(2)为综合利用炉气中的大量SO2,下列方案合理的是???????????。
a.用浓硫酸吸收???????? b.用于制备硫酸
c.高空排放???????????? d.用纯碱液吸收制亚硫酸钠
(3)为检验所得矿渣是中是否含有FeO、Fe2O3、CuO、A12O3、SiO2等氧化物,进行了以下实验;
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通入品红溶液中,溶液褪色。由此判断矿渣中一定含有?????????,一定没有??????。
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH溶液,有沉淀产生,静置后取上层清液,通入过量的CO2溶液变浑浊。由此判断出矿渣中含有?????????,写出通入过量的CO2所发生反应的离子方程式:??????????????。
③取另一份溶液A加入过量的铁粉充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有?????????????,写出此步操作中得到红色物质所发生反应的离子方程式????????????。
参考答案: 本题解析:略
本题解析:略
本题难度:一般