22.30
则消耗NaOH标准溶液的体积平均为???????????,该样品中氮的质量分数为?????????。
参考答案:(18分)
⑴①250 mL容量瓶、胶头滴管、烧杯、玻
本题解析:略
本题难度:一般
2、实验题 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用于消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表

参考答案:![]() 本题解析: 本题解析:
本题难度:一般
3、实验题 保护环境是全球关注的问题。
Ⅰ.某环保部门处理含CN-电镀废水的方法如图(CN-的CNO-中的N的化合价均为-3价):

某学习小组依据上述方法,用下图实验装置进行该电镀废水处理的研究。
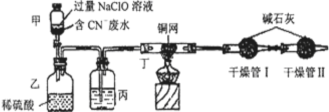
操作步骤:
i.先关闭装置甲的开关,再将含CN-废水与过量NaClO溶液混合,取200mL混合液(其中c(CN-)为0.200mol・L-1)加到装置甲中,塞上橡皮塞。
ii.装置甲中,充分反应后,打开橡皮塞和开关,使溶液全部流入装置乙中,关闭开关。
iii.测定干燥管I增加的质量。
(1)写出装置乙中反应的离子方程式:????????????????????????。
(2)装置丙中的试剂是?????????,装置丁的作用是?????????????????。
(3)假定上述实验中的气体都被充分吸收。若干燥管I增重1.408g。则CN-被处理的百分率为??????????。
(4)你认为用此装置进行实验,与(3)对比,CN-被处理的百分率将?????????(填“偏高”、“偏低”、“无法确定”或“无影响”)。简述你的理由:????????????????。
Ⅱ.防治空气污染,燃煤脱硫很重要。目前,科学家对Fe3+溶液脱硫技术的研究已取得新成果。
(5)科学研究表明,脱硫率与Fe3+浓度、pH关系如图1、2。
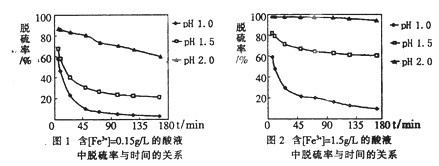
为达到最佳脱硫效果,应采取的适合[Fe3+]及pH分别是????????、????????。
(6)某学习小组为了探究“SO2与Fe3+反应的产物”,将过量的SO2通入FeCl3溶液后,各取10mL反应液分别加到编号为A、B、C的试管中,并设计后续实验的3个方案:
方案①:A中加入少量KMnO4溶液,紫红色褪去。
方案②:B中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:C中加入稀盐酸酸化的BaCl2溶液,产生白色沉淀。
上述实验方案中不合理的是??????????。
参考答案:(16分)(1)2CNO―+6ClO―+8H+=N2↑+2C
本题解析:
试题分析:(1)由电子、电荷、原子守恒可知,乙中反应式为2CNO―+6ClO―+8H+=N2↑+2CO2↑+3Cl2↑+4H2O;(2)丙的目的是除去水分,其中所盛液体为浓硫酸;丁的目的是吸收混合气中的氯气,防止污染环境;(3)I吸收1.408gCO2,由m/M可知,n(CO2)=1.408g÷44g/mol=0.032mol,由2CNO―+6ClO―+8H+=N2↑+2CO2↑+3Cl2↑+4H2O可知,n(CNO―)=n(CO2)=0.032mol,则被处理的n(CN―)=n(CNO―)=0.032mol,由cV可知,总的n(CN―)=0.200mol・L-1×0.2L=0.04mol,则CN―被处理的百分率为0.032mol÷0.04mol×100%=80.0%;(4)本小题为开放题,①偏高的理由:部分Cl2在装置丁没有被吸收而在干燥管I中被吸收;②偏低的理由:部分Cl2残留在装置内没有在干燥管I中被吸收;③无法确定的理由:部分Cl2在干燥管I中被吸收,部分CO2没有在干燥管I中被吸收;(5)读图可知,其他条件相同时,Fe3+浓度越大,脱硫率越高;pH越小,脱硫率越低;故Fe3+浓度为1.50g/L、pH=2.0时,脱硫率最佳;(6)过量的SO2和反应产生的Fe2+都具有还原性,都能使酸性高锰酸钾溶液褪色,方案①不合理。
本题难度:一般
4、选择题 工业上用洗净的废铜片作原料制备硝酸铜,为了节约原料和防止污染环境,宜采用的方法是( )
A.Cu+HNO3(浓)
B.Cu+HNO3(稀)
C.Cu+O2再加HNO3
D.Cu+H2SO4(浓)再加Ba(NO3)2
参考答案:A.浓硝酸与铜反应,制备1molCu(NO3)2,需要4mo
本题解析:
本题难度:简单
5、实验题 (16分)为了研究某土壤样品的酸碱性,某同学25℃时做了如下实验:①取m g土壤于烧杯中,加入VmL的蒸馏水,充分搅拌,静置后过滤,测定滤液的pH。②向滤液中滴加氨水,每加入2 mL氨水就搅拌均匀并测量溶液的pH。根据所得实验记录,以加入的氨水体积为横坐标、pH为纵坐标绘制曲线图如下:
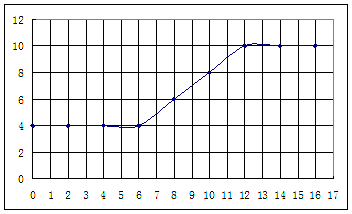
利用上述记录的数据,回答下列问题:(1)所测土壤显 性(填酸、碱、中)(2)已知25℃时, 所用氨水的浓度= 6.0?10-4mol/L,氨水的电离常数K = ???????,为使该滤液呈中性,所加入氨水的恰当体积是????????????????????????。(4)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。下列示意图中,曲线①是用NH3・H2O溶液滴定HCl溶液时,滴加NH3・H2O溶液体积与溶液电导率的关系。请你继续在该图中画出用NH3・H2O溶液滴定CH3COOH溶液时的曲线。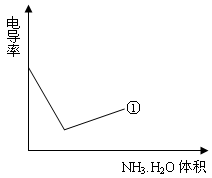
参考答案:(16分) (1) 酸性(2分),(2)?1.7?10-5m
本题解析:略
本题难度:简单
|