D
I
CaCO3
稀盐酸
Na2CO3
稀硫酸
Zn
稀盐酸
Cu
稀硫酸
II
Ca(OH)2
NaOH
AgNO3
Ba(OH)2
A.A
B.B
C.C
D.D
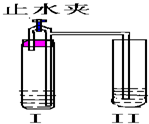
参考答案:A.打开止水夹时,I中碳酸钙和盐酸反应会生成气体二氧化碳,Ⅱ
本题解析:
本题难度:一般
2、实验题 (15分)氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN―等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
I.查阅资料:含氰化物的废水破坏性处理方法。
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
II.实验验证:破坏性处理CN-的效果。
化学兴趣小组的同学在密闭系统中用图10装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
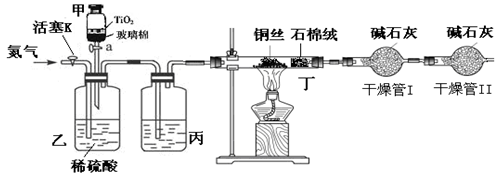
步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol・L―1)倒入甲中,塞上橡皮塞。
步骤3:????????????????????????????????????
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式???????。
(2)完成步骤3?????????????。
(3)丙装置中的试剂是??????????,丁装置的目的是??????????????。
(4)干燥管Ⅱ的作用是????????????????????。
(5)请简要说明实验中通入N2的目的是?????????????。
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为??????。
参考答案:(1)2CNO―+6ClO―+8H+=2CO2↑+N2↑+C
本题解析:(1)次氯酸钠具有强氧化性,能把CNO―氧化生成氮气和CO2,所以反应式为2CNO―+6ClO―+8H+=2CO2↑+N2↑+Cl2↑+4H2O。
(2)由于需要通过加热的铜丝吸收氯气,所以应该先点燃丁处的酒精灯。
(3)因为生成的气体需要干燥,所以丙装置中应该盛放浓硫酸,干燥CO2气体。
(4)干燥管I是吸收CO2的,因此为了防止空气中的水和CO2进入干燥管I中影响对CO2的测量,需要再连接1个干燥管。
(5)由于装置中会残留部分CO2,所以通入氮气的目的是使装置中的CO2全部到干燥管I中被吸收,减少误差。
(6)干燥管Ⅰ中碱石灰增重1.408g,则反应中生成的CO2是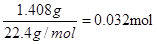 ,所以CNO―的物质的量是0.032mol。CN-的总的物质的量是0.04mol,所以根据原子守恒可知,该实验中测得CN-被处理的百分率为80%。 ,所以CNO―的物质的量是0.032mol。CN-的总的物质的量是0.04mol,所以根据原子守恒可知,该实验中测得CN-被处理的百分率为80%。
本题难度:一般
3、填空题 某校化学研究学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。按右图装置进行实验,已知B中盛放的是浓硫酸。并回答以下问题。
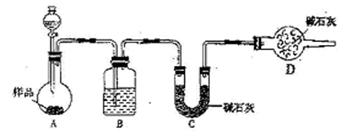
(1)实验加入药品前应先?????????????。分液漏中应该装??????(填:盐酸或硫酸)。
D装置的作用是??????????????????????。
(2)实验中除称量样品质量外,还需称???????????????????装置前后质量的变化。
参考答案:
(1)检查装置的气密性(2分)硫酸(2分)防止空气中
本题解析:略
本题难度:一般
4、实验题 (16分)硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。

(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:
?????????????????????????????????????????????????????????????????。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种:?????????????。
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量?????????????
(填“偏高”、“偏低”或“无影响”)。
乙方案:实验步骤如以下流程图所示:
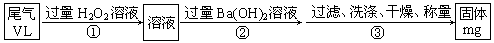
(4)写出步骤②中反应的化学方程式?????????????????????????????????。
(5)步骤③中洗涤沉淀的方法是?????????????????????????????????????。
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为????????????????????????????(用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与方案乙相同。
(7)你认为丙方案是否合理,说明理由:
?????????????????????????????????????????????????????????????????。
参考答案:(1)增大气体与溶液的接触面积,有利于SO2与碘水充分反应(
本题解析:甲.(1)根据多孔球泡D的结构可知可以增大反应物的接触面积,使反应更充分。
(2)SO2具有还原性,还是一种酸性氧化物,所以可以用酸性高锰酸钾溶液或碱液等。
(3)没有及时关闭活塞A,则通过的气体就偏多,测定结果就偏低。
乙.(4)双氧水具有氧化性,可以把SO2氧化生成硫酸,而双氧水被还原生成水。所以在反应②就是硫酸和氢氧化钡的中和反应。
(5)沉淀应该在过滤器中进行,具体操作是向漏斗里注入蒸馏水,使水面没过沉淀物,待水流尽后,重复操作2~3次。
(6)硫酸钡是mg,则根据硫原子守恒可知SO2的物质的量是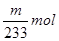 。所以SO2的体积分数是 。所以SO2的体积分数是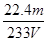
丙.(7)由于SO2和氢氧化钡反应生成的亚硫酸钡易被氧化生成硫酸钡,因此最后得到的固体是混合物,所以方案是不正确的。
本题难度:一般
5、实验题 工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(含少量碳元素)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是_________________。
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中有Fe2+,应先用________(选填序号)。
a.KSCN溶液和氯水b.铁粉和KSCN溶液 c.浓氨水d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量 BaCl2溶液,经适当操作后得到干燥固体2.33g。由此推知气体Y中SO2的体积分数为____。
[探究二] 分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
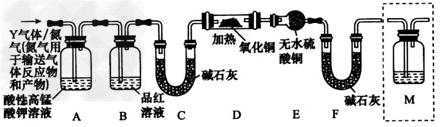
(3)装置B中试剂的作用是____________。
(4)认为气体Y中还含有CO2的理由是__________ (用化学方程式表示)。
(5)为确认CO2的存在,需在装置中添加M于____(填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是___________________
参考答案:(1)铁钉遇冷浓硫酸发生了钝化(或其他合理答案)
(
本题解析:
本题难度:一般
|