微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如下图,下列判断错误的是

A.a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液
B.a点对应的Ksp不等于c点对应的Ksp
C.b点将有沉淀生成,平衡后溶液中c(SO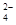 )一定等于3×10-3 mol・L-1
)一定等于3×10-3 mol・L-1
D.向d点溶液中加入适量CaCl2固体可以变到c点
参考答案:BC
本题解析:
试题分析:A、处于曲线上的点为饱和溶液的平衡状态,故A正确;B、a、c两点温度相同,Ksp是一常数,温度不变Ksp不变,在曲线上的任意一点Ksp都相等,故B不正确;C、根据图示数据,可以看出b点Qc=2×l0-5>Ksp,所以会生成沉淀,平衡向生成沉淀的方向进行,此时溶液中c(SO4-)会小于4×l0-3mol/L,由于c(Ca2+)>c(SO42-),则c(SO4-)小于3×l0-3mol/L,故C不正确;D、d点为不饱和状态,钙离子浓度较小,如加入适量CaCl2固体,钙离子浓度增大,此时硫酸根
本题难度:一般
2、填空题 医学上在进行胃肠疾病的检查时,利用X射线对BaSO4穿透能力较差的特性,常用BaSO4做内服造影剂,这种检查手段称为钡餐透视。
(1)请写出BaSO4能作为钡餐透视的另外一个理由:________________________。
(2)请用文字叙述和离子方程式说明钡餐透视时为什么不用BaCO3?_________________________。
(3)某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:
①5 mL水 ②20 mL 0.5 mol・L-1的Na2SO4溶液 ③40 mL 0.2mol・L-1的Ba(OH)2溶液 ④40 mL 0.1 mol・L-1的
H2SO4溶液中,溶解至饱和。
①以上各溶液中,c(Ba2+)的大小顺序正确的是__________,BaSO4的溶解度的大小顺序为_________(填序号)。
A.③>①>④>② B.③>①>②>④ C.①>④>③>② D.①>③>④>②
②已知25℃时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液③中的c(SO42-)为__________,溶液②中
c(Ba2+)为__________________。
③某同学取同样的溶液③和溶液④直接混合,则混合溶液的pH为__________(假设混合后溶液的体积为混合前两溶液的体积之和)。
参考答案:(1)BaSO4既不溶于水,也不溶于酸,可经人体排出体外,不
本题解析:
本题难度:一般
3、填空题 许多在水溶液中的反应,往往有易溶物转化为难溶物或难溶物转化为更难溶物的现象。下表为相同温度下某些物质的溶解度。
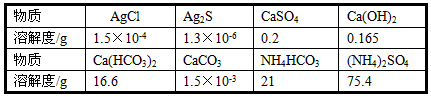
(1)若在有氯化银固体的水中加入硫化钠溶液,可能发生的现象是__________________。
(2)生成硫酸铵化肥的方法之一是:把石膏粉(CaSO4)悬浮于水中,不断通入氨气并通入适量的二氧化碳,充分反应后立即过滤,滤液经蒸发而得到硫酸铵晶体,写出该反应的化学方程式__________________。
参考答案:(1)白色固体消失,同时会生成黑色固体
(2)CaS
本题解析:
本题难度:一般
4、简答题 金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的.难溶金属的氢氧化物在不同pH下的溶解度(s,mol-L-1)见图.
(1)pH=3时溶液中铜元素的主要存在形式是:______.(写化学式)
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为______.(填字母)
A、<1?????B、4左右?????C、>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,______(能、不能)通过调节溶液pH的方法来除去,理由是______.
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式.______.
(5)已知一些难溶物的溶度积常数如下表.
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS
Ksp
6.3×10-18
2.5×10-13
1.3×10-36
3.4×10-28
6.4×10-53
1.6×10-24
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的______除去它们.
A、NaOH???? ?B、FeS???? ?C、Na2S (选填序号)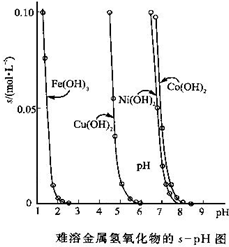
参考答案:(1)由图可知,在pH=3时,溶液中不会出现Cu(OH)2沉
本题解析:
本题难度:一般
5、填空题 (16分)Na2CO3俗称纯碱、苏打,NaHCO3俗称小苏打,两者在日常生活和工业生产中都有着广泛的应用。某化学兴趣小组设计了如下实验来探究两者的某些性质。请你根据所学知识帮他们完成有关的设计和实验。
(1)甲同学测定两者的酸碱性:各取一定量的固体溶于水,配成相同浓度的溶液,测定其pH值,测定结果为Na2CO3、NaHCO3的pH分别为a和b(a、b均大于7),则a b(填“大于”“等于”或“小于”),测定溶液的pH值所用的主要仪器有:pH试纸、表面皿、 和标准比色卡。
(2)有关①100mL0.1 mol・L-1NaHCO3、 ②100mL0.1 mol・L-1Na2CO3,两种溶液的叙述不正确是
A.NaHCO3溶液中:c (H+)+c (Na+)=" c" (HCO3-)+2c(CO32-)+c(OH-)
B.Na2CO3溶液中:2c (Na+)=" c" (HCO3-)+c(CO32-)+c(H2CO3)
C.①溶液中:c(CO32-)>c(H2CO3)
D.②溶液中:c(HCO3-)>c(H2CO3)
(3)乙同学取一定量的碳酸钠溶液于试管中,滴加2~3滴酚酞试液,发现溶液变红,继续滴加BaCl2溶液,预计可观察到 ,请你结合必要的离子方程式,应用平衡的观点解释有关现象的产生: 。
(4)丙同学往10mL0.10 mol・L-1的Na2CO3溶液中逐滴滴加0.10 mol・L-1的HCl,当溶液中的:
c(Na+)=c(Cl-)+c(HCO3-)+2c(CO32-),此时溶液呈 (填“酸性”、“中性”或“碱性”),所用HCl的体积 10mL。(填“大于”“等于”或“小于”)
(5)已知:Ksp(CaCO3)=4.96×10-9,不考虑其它因素影响,现将0.40 mol・L-1的Na2CO3溶液和0.20 mol・L-1的CaCl2溶液等体积混合,则混合后溶液中Ca2+浓度为 mol・L-1。
参考答案:21.(16分) (每空2分)
(1)大于
本题解析:
试题分析:(1)组成盐的酸根对应的酸越弱,该盐的水解程度越大,等浓度、等体积的Na2CO3和NaHCO3混合液中,碳酸根的水解程度大于碳酸氢根的水解程度,水解程度越大,碱性越强,PH越大,Na2CO3、NaHCO3的pH分别为a和b,则a大于b,测定溶液的pH值基本操作为用镊子撕一块试纸放在干净的表面皿上,用玻璃棒蘸取待测液,滴在试纸的中央,变色后与标准比色卡对比,读出PH值,则所用的主要仪器有:pH试纸、表面皿、玻璃棒和标准比色卡。
(2)A.NaHCO3溶液中存在电荷守恒,为c (H+)+c (Na+)=" c" (HCO3-)+2c(CO32-)+c(OH-),正确;B.Na2CO3溶液中存在物料守恒为c (Na+)=" 2c" (HCO3-)+2c(CO32-)+2c(H2CO3),错误;C.NaHCO3溶液显碱性,HCO3-水解程度大于其电离程度,水解产生H2CO3,电离产生CO32-,所以c(CO32-)<c(H2CO3) ,错误;D.碳酸钠溶液,阴离子分步水解,第一步水解程度(生成HCO3-)大于第二步水解程度(生成H2CO3),所以:c(HCO3-)>c(H2CO3),正确;选BC。
(3)由于CO32- + H2O  HCO3-+OH-,CO32-水解导致碳酸钠溶液显碱性,滴加酚酞试液,溶液变红色,继续滴加BaCl2溶液,发生Ba2+ +CO32-=BaCO3↓(白色沉淀),水解平衡逆向移动,碱性减弱,OH-浓度减少,红色褪去。 HCO3-+OH-,CO32-水解导致碳酸钠溶液显碱性,滴加酚酞试液,溶液变红色,继续滴加BaCl2溶液,发生Ba2+ +CO32-=BaCO3↓(白色沉淀),水解平衡逆向移动,碱性减弱,OH-浓度减少,红色褪去。
(4)任何溶液均呈电中性,根据电荷守恒,c(Na+)+c(H+)= c(Cl-)+c(HCO3-)+2c(CO32-)+c(OH-),已知溶液中存在c(Na+)= c(Cl-)+c(HCO3-)+2c(CO32-),所以c(H+)= c(OH-),此时溶液呈中性,往10mL0.10 mol・L-1的Na2CO3溶液中逐滴滴加0.10 mol・L-1的HCl10mL,溶液恰好反应生成NaHCO3,碳酸氢钠溶液显碱性,若要使溶液呈中性,需多加盐酸,所以所用HCl的体积大于10mL。
(5)将0.40 mol・L-1的Na2CO3溶液和0.20 mol・L-1的CaCl2溶液等体积混合,设体积为1L,发生反应Na2CO3 +CaCl2=CaCO3↓+2NaCl
0.2 0.2
剩余碳酸钠的物质的浓度为(0.4-0.2)/2=0.1mol/L,已知Ksp(CaCO3)=4.96×10-9,则0.1×c(Ca2+)= 4.96×10-9,解得c(Ca2+)= 4.96×10-8,则混合后溶液中Ca2+浓度为4.96×10-8mol・L-1。
考点:考查盐类水解PH值的判断,电解质溶液中的离子平衡,沉淀溶解平衡的应用等知识。
本题难度:困难
|