��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ȥ�����������������������ʣ��±��г��ӷ�����ȷ����
ѡ��
| ��?��
| ��������
| �����ʵķ���
|
A
| ����ͭ
| �Ȼ���
| ��ˮ�ܽ⡢���ˡ������ᾧ
|
B
| ����
| ˮ����
| ͨ��ʢ��Ũ�����ϴ��ƿ
|
C
| ��������Һ
| ϡ����
| �������̼������Һ������
|
D
| ������̼
| һ����̼
| ��ȼ
�ο��𰸣�B
���������
���������A�ֻ���ܽ⡢���˾����ˣ��ʴ���C��D������µ����ʣ��ʴ�����ѡB��
����������һ�������ַ����������ʳ��׳�ȥ������ת��Ϊ�����ʣ���ѡ���ʲ����������ʷ�����Ӧ��Ҳ��Ҫ�ڳ�ȥ���ʵ�ͬʱ�ֻ������������ʡ�
�����Ѷȣ���
2������� ��8�֣���һ����ɫ���壬�����ɣ�CuSO4��Na2SO4��Na2CO3��Ba(NO3)2��NaCl �е�һ�ֻ�����ɡ�Ϊ���ж����еijɷݣ�ijͬѧ���������ʵ�鷽������ ������ʵ������ļ��裬�������������Щ������һЩ�жϣ� ������ʵ������ļ��裬�������������Щ������һЩ�жϣ�
ʵ�鲽��
| ʵ������
| ��??????��
| ȡ��������ˮ
| ����ֻ�õ���ɫ��Һ
| һ��û��____________________________��
| �����а�ɫ���������ã��ϲ���Һ��ɫ
| һ��û��___________________________��
| ȡ�ڵĻ�
�������
| ���ڳ����м������ᣬ���������ܽ⣻���ˣ�����Һ�м���AgNO3��Һ��ϡ���ᣬ�а�ɫ����
| һ������_____________________________��
�����м�����������ӷ���ʽ��
_______________________________________��
�ܷ�ȷ��ԭ�������Ƿ���NaCl����˵������
_______________________________________
_______________________________________��
?
�ο��𰸣�
ʵ�鲽��
ʵ������
��??????��
�����������
�����Ѷȣ�һ��
3��ʵ���� ��8�֣�MnO2��һ����Ҫ�������ܲ��ϣ���MnO2���ᴿ�ǹ�ҵ��������Ҫ���ڡ�ij�о���ѧϰС������˽���MnO2�����н϶��MnO��MnCO3����Ʒת��Ϊ��MnO2��ʵ�飬���������£�
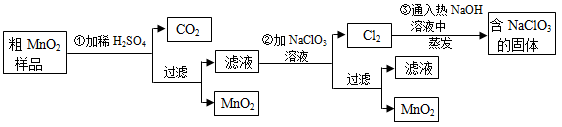
��1���ڢٲ���ϡH2SO4ʱ����MnO2��Ʒ�е�?????????��д��ѧʽ��ת��Ϊ���������ʡ�
��2���ڢڲ���Ӧ�����ӷ���ʽ�ǣ�
??????��?ClO3����??????��?MnO2����?Cl2����??????��
��3���ڢ۲������������������������̨������Ȧ����???????��???????����������
��4������MnO2��Ʒ������Ϊ12.69g���ڢٲ���Ӧ�����˵õ�8.7g MnO2�����ռ���0��224LCO2����״���£������ڵڢٲ���Ӧ��������Ҫ???????mol H2SO4��
����֪Ħ��������MnO2 -87g/mol��? MnO-71g/mol��?? MnCO3-115 g/mol��
�ο��𰸣���8�֣�
��1��MnO��MnCO3��2�֣���һ��1�֣�
�����������1����Ʒ��ϡ�����MnO2���ܣ���MnO��MnCO3���������У�
MnCO3��H2SO4=MnSO4��H2O��CO2��???? MnO��H2SO4=MnSO4��H2O
���˺�õ�MnSO4��Һ
��2����ͼʾ��֪��NaClO3�е���Ԫ�ػ��ϼ۽�Ϊ0��������������������������Һ�е�MnSO4����������ΪMnO2��5Mn2++2ClO3-+4H2O=5MnO2��+Cl2��+8H+
��3��������Ҫ����������������̨�������ƾ��ơ���������
��4������������ʽ�ɼ������MnCO3Ϊ0.01mol������Ϊ1.15g��������0.01mol�����ᣬ�����ɼ����MnOΪ2.84g��Ҳ����0.04mol��������0.04mol�������������Ҫ��������ʵ���Ϊ0.05mol
�����Ѷȣ�һ��
4��ѡ���� �ܼ���Mg��AgNO3��Na2CO3��NaAlO2������Һ���Լ���
A��HNO3
B��KOH
C��BaCl2
D��NaClO
�ο��𰸣�A
�����������
�����Ѷȣ���
5��ѡ���� ij��Һ�к��нϴ�����Mg2+��Ag+��Ba2+ ���������ӣ���������������һ�������������м����Լ���˳���У���ȷ����
��NaOH��Һ��NaCl��Һ��Na2SO4��Һ??? ��NaOH��Һ��Na2SO4��Һ��NaCl��Һ
��NaCl��Һ��Na2SO4��Һ��NaOH��Һ???? ��NaCl��Һ��NaOH��Һ��Na2SO4��Һ
A���٢ڡ���
B���ۢ� ��
C���٢ۡ�
D���ڢ�
�ο��𰸣�B
���������
��ȷ�𰸣�B
OH�D SO42�D����ʹ�������ӳ����������ȼ�NaCl����ȥAg�����ȼ�OH�D��SO42�D���ɡ�
�����Ѷȣ�һ��
|
|