微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列除去杂质的实验方法正确的是:?
A.除去CO中少量O2:通过灼热的Cu网后收集气体
B.除去K2CO3固体中少量NaHCO3:置于坩埚中加热
C.用过量氨水除去Al3+溶液中的少量Fe3+
D.除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后放置
2、选择题 利用下列实验装置能完成相应实验的是
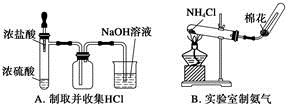
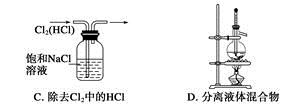
3、实验题 工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产Zn(NO3)2・6H2O晶体,其工艺流程为:
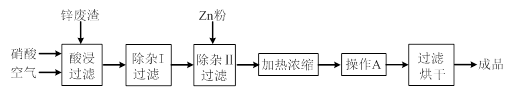
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
氢氧化物
| Al(OH)3
| Fe(OH)3
| Fe(OH)2
| Cu(OH)2
| Zn(OH)2
|
开始沉淀的pH
| 3.3
| 1.5
| 6.5
| 4.2
| 5.4
|
沉淀完全的pH
| 5.2
| 3.7
| 9.7
| 6.7
| 8.0
?
(1)在“酸浸”步骤中,为提高锌的浸出速率,除通入空气“搅拌”外,还可采取的措施是??????。
(2)在“除杂I”步骤中,需再加入适量H2O2溶液,目的是将Fe2+氧化为?????,便于调节溶液的pH使铁元素转化为氢氧化物沉淀除去。为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为 ???????~??????。检验Fe3+是否沉淀完全的实验操作是静置片刻,取少量上层清液,滴加????????????溶液,若不出现血红色,表明Fe3+沉淀完全。
(3)加入Zn粉的作用是除去溶液中的??????????。
4、选择题 0.5 molNa3PO4中所含有的离子数目为
A.6.02×1023
B.3.01×1023
C.1.204×1024
D.1.204×1023
5、选择题 下列操作不能达到目的是( ) | 选项 | 目的 | 操作
A.
配制100 mL 1.0 mol/L CuSO4溶液
将25 g CuSO4?5H20溶于100 mL蒸馏水中
B.
除去KNO3中少量NaCl
将混合物制成热的饱和溶液,冷却结晶,过滤
C.
在溶液中将MnO4-完全转化为Mn2+
向酸性KMnO4溶液中滴加H2O2溶液至紫色消失
D.
确定NaCl溶液中是否混有Na2CO3
取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊
A.A
B.B
C.C
D.D
|
|