微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列事实不能用勒夏特列原理解释的是
A.收集氯气用排饱和食盐水的方法
B.加催化剂,使N2和H2在一定的条件下转化为NH3
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.加压条件下有利于SO2和O2反应生成SO3
参考答案:B
本题解析:加催化剂,使N2和H2在一定的条件下转化为NH3,没有利用勒夏特列原理解。
本题难度:一般
2、填空题 830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g) ?CO2(g)+H2(g);△H<0??试回答下列问题:
?CO2(g)+H2(g);△H<0??试回答下列问题:
(1)若起始时c(CO)="2" mol?L-1,c(H2O)="3" mol?L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=???????????.
(2)在相同温度下,若起始时c(CO)="1" mol?L-1,c(H2O)="2" mol?L-1,反应进行一段时间后,测得H2的浓度为0.5 mol?L-1,则此时该反应是否达到平衡状态 ???????(填“是”与“否”),?此时v(正)????????v(逆)(填“大于”“小于”或“等于”),你判断的依据是???????????
?????????????????????????????????????????????????????????。
(3)若降低温度,该反应的K值将??????????????(均填“增大”“减小”或“不变”)。
参考答案:(1)平衡常数k=1
(2)否??大于?依据是Q=0.
本题解析:
试题分析:(1)???? CO(g)+H2O(g) ?CO2(g)+H2(g)
?CO2(g)+H2(g)
起始浓度(mol/L)??? 2????? 3???????????? 0????? 0
之和浓度(mol/L)?? 1.2??? 1.2?????????? 1.2???? 1.2
平衡浓度(mol/L)?? 0.8??? 1.8?????????? 1.2???? 1.2
所以平衡常数K=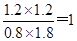
(2)在相同温度下,若起始时c(CO)="1" mol?L-1,c(H2O)="2" mol?L-1,反应进行一段时间后,测得H2的浓度为0.5 mol?L-1,则根据方程式可知,此时CO2的浓度也是0.5mol/L,而CO和水蒸气的浓度分别是0.5mol/L和1.5mol/L,则此时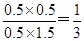 <1,所以反应没有达到平衡状态。此时正反应速率大于逆反应速率。
<1,所以反应没有达到平衡状态。此时正反应速率大于逆反应速率。
(3)正反应是放热反应,则降低温度,平衡向正反应方向进行,所以该反应的K值将增大。
点评:该题是高考中的常见题型和重要的考点,属于中等难度的试题。试题贴近高考,基础性强,侧重对学生灵活运用基础知识解决实际问题的能力的培养。该题的关键是明确平衡常数的含义、计算依据以及影响因素,如何结合题意灵活运用即可。有利于调动学生的学习兴趣,提高学生的应试能力。
本题难度:一般
3、选择题 一定温度下,在固定体积的密闭容器中进行反应:N2+3H2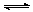 2NH3。该反应达到平衡的标志是
2NH3。该反应达到平衡的标志是
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时生成3m mol H2
C.混合气体的密度不再随时间变化
D.容器内的总压强不再随时间而变化
参考答案:D
本题解析:略
本题难度:一般
4、填空题 在400℃,1.01×105Pa时,将SO2和14molO2?压入一个装有催化剂的V升密闭反应器中,发生2SO2+O2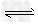 2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2:
2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2:
(1)SO2的起始浓度为_______,SO3(气)的平衡浓度为_________;
(2)SO2的转化率为________,O2的平均反应速率为________;
(3)平衡时SO3(气)占总体积的百分数为__________,此时体系压强为反应起始时体系压强的________倍;
(4)达平衡后再加入2molSO2、12molO2和4molSO3(气),此时正反应速率将_______,逆反应速率将_______,平衡_______移动。
参考答案:(1)6/Vmol・L-1 ;4/Vmol・L-1
本题解析:
本题难度:一般
5、计算题 在2 L密闭容器中,充入1 mol N2和3mol H2,在一定条件下发生合成氨反应,2 min时达到平衡。测得平衡混合气中NH3的体积占25%,求:
(1)v(H2)
(2)N2的转化率
(3)H2在平衡时的体积分数
(4)平衡时容器的压强与起始时压强之比
参考答案:(1)v(H2) =3×0. 4 mol/(2L×2min)
本题解析:
本题难度:一般