微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:Cu+2Fe3+═2Fe2++Cu2+.现把相同物质的量的CuSO4、FeCl3和Zn置于水中充分反应,反应所得混合物中除含有SO42-和Cl-外,还含有
A.Zn2+、Cu、Fe3+
B.Zn、Cu2+、Fe3+
C.Zn2+、Cu2+、Fe2+
D.Zn2+、Cu、Cu2+、Fe2+
参考答案:D
本题解析:分析:根据金属活动性反应的先后顺序:在金属活动性顺序中,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来,所以,先是Zn与FeCl3反应,接着是Zn与CuSO4反应,据此即可解答.
解答:把相同物质的量的CuSO4、FeCl3和Zn置于水中充分反应,设它们的物质的量都为1mol,根据反应顺序判断:
先是? Zn+2FeCl3=ZnCl2+2FeCl2,Zn+CuSO4 =ZnSO4 +Cu
??? 0.5mol??? 1mol???????????????? 0.5mol???0.5mol????
剩余0.5molZn,剩余0.5molCuSO4,生成??0.5molCu,
反应所得混合物中除含有SO42-和Cl-外,还含有Zn2+、Cu、Cu2+、Fe2+,
故选:D.
点评:本题考查了金属活动性顺序的应用,依据金属活动性顺序的意义进行解答是关键,题目较简单.
本题难度:困难
2、选择题 下列说法中,正确的是( )
A.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
B.钢铁设备与外加直流电源的正极相连可以防止钢铁腐蚀
C.氮的固定只有在高温、高压、催化剂的条件下才能实现
D.高纯度的硅单质广泛用于制作光导纤维
参考答案:A、金属铝表面的氧化物薄膜阻止铝继续反应,对内部金属起保护作
本题解析:
本题难度:一般
3、选择题 下列物质中,属于含有共价键的离子化合物的是(??? )
A.MgCl2
B.Br2
C.KOH
D.H2S
参考答案:C
本题解析:A项MgCl2是离子化合物,但其中不含共价键。B项中Br2只含共价键,且是单质。D项中H2S只含共价键,是共价化合物。C项中KOH是离子化合物,其中O原子与H原子之间以共价键结合,符合题意。
本题难度:简单
4、选择题 最近,科学家冶炼出纯度高达99.999 %的铝,你估计它具有性质是?(???)
A.熔点比铁铝合金小
B.在冷、浓HNO3中可以钝化
C.在空气中放置容易生锈,进而被腐蚀
D.当它与铁的粉碎粒度相同时,与4mol/L盐酸反应速率比纯铁大
参考答案:BD
本题解析:合金的熔点一般低于它的成分金属,A不正确。铝表面容易被氧化生成一层致密的氧化膜,从而阻止继续被氧化,所以铝制容器耐腐蚀,C不正确。铝的金属性强于铁的,所以选项BD正确。答案选BD。
本题难度:一般
5、填空题 铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下:
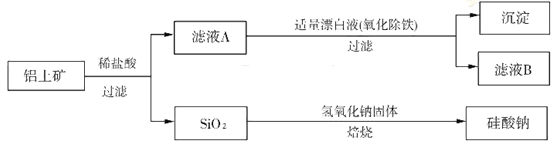
(1)滤液A所含溶质属于盐的是___________________。
(2)检验滤液B中是否还含有铁元素的方法为:_______________________________________
____________________________________________________________(注明试剂、现象)。
(3)将滤液B中的铝元素以沉淀形式析出,最佳试剂应选_____________(填代号)。
a.氢氧化钠溶液? b.硫酸溶液? c.氨水? d.二氧化碳
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___________(填代号)。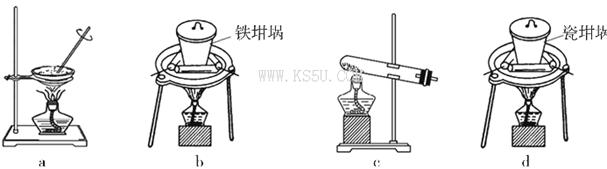
参考答案:(1)AlCl3、FeCl2(2)取少量滤液B,加入KSCN
本题解析:
试题分析:(1)铝土矿和盐酸的反应为Al2O3+6HCl=2AlCl3+3H2O FeO+2HCl=FeCl2+H2O,所以滤液A所含溶质属于盐的是AlCl3、FeCl2;(2)滤液B中可能含有的铁元素以Fe3+形式存在,检验方法为:取少量滤液B,加入KSCN溶液,若不变红,再加入氯水,仍然不变红,说明滤液B中不含铁元素。(3)滤液A经氧化Fe2+转化为Fe3+,除去Fe3+后滤液B的主要成分为AlCl3溶液,要使铝元素转化为氢氧化铝沉淀最佳试剂为氨水;(4)固体的焙烧应用坩埚,氢氧化钠和陶瓷的成
本题难度:一般