微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 物理量的符号及其单位都正确的是
A.阿伏加德罗常数:NA,mol
B.摩尔质量:M,g?mol-1
C.气体摩尔体积:Vm,mol?L-1
D.物质的量浓度::C,L?moL-1
参考答案:B
本题解析:分析:根据各物理量的定义解答该题.
解答:A、阿伏加德罗常数0.012kg12C中所含的原子数目叫做阿伏加德罗常数,阿伏加德罗常数的符号为NA,阿伏加德罗常的近似值为:6.02×1023/mol,故A错误;
B、摩尔质量为单位物质的量的物质的质量,符号为M,单位是g?mol-1,故B正确;
C、气体摩尔体积为一定条件下的单位物质的量的气体的体积,表达式为Vm= ,符号为Vm,单位为L/mol,故C错误;
,符号为Vm,单位为L/mol,故C错误;
D、物质的量浓度为单位体积溶液含有溶质的物质的量,表达式为=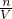 ,符号为C,单位为mol/L,故D错误.
,符号为C,单位为mol/L,故D错误.
故选B.
点评:本题考查常见物理量的了解,题目难度不大,注意基础知识的积累.
本题难度:困难
2、选择题 用NA表示阿伏加德罗常数的值.下列说法正确的是
A.1?molS2-中含有的电子数为2NA
B.1?L?1mol?L-1Na2SO4溶液中含有的钠离子数为NA
C.常温常压下,22.4?LC12中含有的分子数为NA
D.常温常压下,32?gO2中含有的分子数为NA
参考答案:D
本题解析:分析:A、一个硫离子含有18个电子;
B、依据n=cV计算溶质物质的量结合化学式计算离子数;
C、依据气体摩尔体积的条件应用分析判断;
D、依据n= 计算物质的量计算分子数.
计算物质的量计算分子数.
解答:A、1 molS2-中含有的电子数为18NA,故A错误;
B、1 L 1mol?L-1Na2SO4溶液中含有的钠离子数为2NA,故B错误;
C、常温常压下,22.4 LC12中物质的量不是1mol,含有的分子数不是NA,故C错误;
D、常温常压下,32 gO2物质的量为1mol,含有的分子数为NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要是物质的量计算微粒数的计算应用,气体摩尔体积的条件应用,题目难度中等.
本题难度:一般
3、选择题 若1gN2中含有x个原子,则阿伏加德罗常数是
A.mol-1
B.mol-1
C.14xmol-1
D.28xmol-1
参考答案:C
本题解析:分析:利用氮气的构成及n=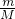 、N=n×NA来计算,即可解答.
、N=n×NA来计算,即可解答.
解答:1gN2的物质的量为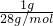 =
= mol,
mol,
又氮气分子是由2个氮原子构成的,
则原子的物质的量为 mol×2=
mol×2=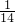 mol,
mol,
由N=n×NA可知,阿伏加德罗常数为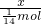 =14xmol-1,
=14xmol-1,
故选C.
点评:本题考查阿伏伽德罗常数的计算,明确质量、微粒数目与物质的量的关系是解答的关键,较简单.
本题难度:困难
4、选择题 用NA代表阿伏加德罗常数,下列说法正确的是?
A.标准状况下,22.4 L CHCl3中含有的氯原子数目为3NA
B.7 g CnH2n中含有的氢原子数目为NA
C.18 g D2O中含有的质子数目为10 91EXAm.orgNA
D.1 L 0.5 mol/L Na2CO3溶液中含有的CO32-数目为0.5NA
参考答案:B
本题解析:试题分析:本题主要考查“阿伏伽德罗常数”的相关应用,是高考中必考的内容,考生在复习时应有意识的加强此类题目的训练。
选项A、标准状态下,CHCl3为液态,因此不可以用气体摩尔体积计算。
选项B、正确。7 g CnH2n的物质的量为
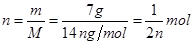 ;因此氢原子的个数
;因此氢原子的个数
为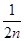 ?×2n=1mol,因此其氢原子数目为NA。
?×2n=1mol,因此其氢原子数目为NA。
选项C、18 g D2O的物质的量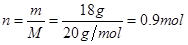 。因此所含的质子数应
。因此所含的质子数应
为0.9mol×10=9mol,为9NA。
选项D、1 L 0.5 mol/L Na2CO3溶液中,n(Na2CO3)="1" L×0.5 mol/L="0.5" mol,应为0.5NA,但是,此时应考虑到CO32-在水中会发生水解,因此CO32-的数目应该小于0.5NA。
考点:阿伏伽德罗常数
点评:本题虽是对阿伏伽德罗定律的考查,但是涉及到的知识点较为全面。解题时应综合各部分的知识点
1.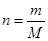 ?????
?????
2.N=c・V
本题难度:简单
5、选择题 取一小块钠放在燃烧匙里加热,下列实验现象描述正确的是
① 钠先熔化???②燃烧放出黄色火花??③燃烧后得到白色固体??④燃烧时火焰为黄色???????⑤燃烧后得到浅黄色固体
A.①②
B.①②③
C.①④⑤
D.①③④
参考答案:C
本题解析:试题分析:钠的熔点较低,受热易熔化。同时钠极易被氧化,加热时燃烧发出黄色的火焰,同时生成淡黄色的过氧化钠,因此正确的答案选C。
考点:考查钠燃烧的有关实验现象
点评:化学是以实验为基础的一门学科,所以准确观察并描述实验现象,也是学生必须具备的一种能力,本题难度不大,较易得分。
本题难度:困难