微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)水溶液中存在多种平衡,请根据所学化学知识回答下列问题:
(1)在浓度均为0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH3.H2O ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为 (填序号)
(2)浓度均为0.1 mol・L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH= 。
参考答案:(1)④>②>①>③;(2)④>②&
本题解析:
试题分析:在四种物质的溶液中存在的大量方程式是:①CH3COONH4= CH3COO-+NH4+;②NH4HSO4=NH4++H++SO42-;③NH3.H2O NH4++OH-;④(NH4)2SO4= 2NH4++ SO42-;在①②④中都存在NH4+发生水解反应的而消耗使离子的浓度减小;①CH3COO-对前者其促进作用,使离子浓度进一步减小,②H+对NH4+发生水解反应其抑制作用;所以②>①.根据物料守恒可知④>②,NH3.H2O是若电解质,电离程度是微弱的,所以其离子浓度远小于盐电离产生的离子浓度,因此①>③。故四种溶液中的离子浓度关系的是④>②>①>③;(2)①硫酸是二元强酸,完全电离;③氢氧化钠是一元强碱,完全电离②醋酸是一元弱酸,部分电离,它们产生的离子对水的电离起抑制作用,电离产生的离子浓度越大,对水的电离的抑制作用就越大,所以对水的抑制作用①>③>②,④氯化铵是强酸弱碱盐,电离产生的NH4+发生水解反应消耗水电离产生的OH-,会促进水的电离作用。所以由水电离出的H+浓度由大到小的顺序是④>②>③>①;(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,n(OH-)=0.1mol,c(OH-)=0.1mol/L,则由于中性溶液的pH=6,所以在该温度下的水的离子积产常数是1×10-12,c(H+)=1×10-12÷0.1mol/L=1×10-11,所以充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=11.
NH4++OH-;④(NH4)2SO4= 2NH4++ SO42-;在①②④中都存在NH4+发生水解反应的而消耗使离子的浓度减小;①CH3COO-对前者其促进作用,使离子浓度进一步减小,②H+对NH4+发生水解反应其抑制作用;所以②>①.根据物料守恒可知④>②,NH3.H2O是若电解质,电离程度是微弱的,所以其离子浓度远小于盐电离产生的离子浓度,因此①>③。故四种溶液中的离子浓度关系的是④>②>①>③;(2)①硫酸是二元强酸,完全电离;③氢氧化钠是一元强碱,完全电离②醋酸是一元弱酸,部分电离,它们产生的离子对水的电离起抑制作用,电离产生的离子浓度越大,对水的电离的抑制作用就越大,所以对水的抑制作用①>③>②,④氯化铵是强酸弱碱盐,电离产生的NH4+发生水解反应消耗水电离产生的OH-,会促进水的电离作用。所以由水电离出的H+浓度由大到小的顺序是④>②>③>①;(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,n(OH-)=0.1mol,c(OH-)=0.1mol/L,则由于中性溶液的pH=6,所以在该温度下的水的离子积产常数是1×10-12,c(H+)=1×10-12÷0.1mol/L=1×10-11,所以充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=11.
考点:考查盐的水解、影响水的电离的各种因素;水的离子积常数及溶液的pH的计算的知识。
本题难度:一般
2、选择题 PH=3和PH=5的盐酸等体积混合后溶液的PH是
A.3.3
B.3
C.5
D.4.7
参考答案:A
本题解析:
试题分析:PH=3的盐酸c(H+)=10-3mol/LPH=5的盐酸中c(H+)=10-5mol/L,等体积混合后
c(H+)=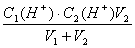 =
= =5.05×10-4mol/lPH=-lg5.05×10-4=4-0.7=3.3,选A。
=5.05×10-4mol/lPH=-lg5.05×10-4=4-0.7=3.3,选A。
考点:考查PH值的计算。
本题难度:一般
3、选择题 对H2O的电离平衡不产生影响的微粒是[???? ]
A.CH3CH2OH??
B.NH4+
C.Cl2??
D.S2-
参考答案:A
本题解析:
本题难度:一般
4、选择题 水的电离过程为H2O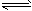 H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=
H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=
2.1×10-14。则下列叙述正确的是[???? ]
A.c(H+)随温度的升高而降低
B.35℃时,c(H+)>c(OH-)
C.溶液:pH(35℃)>pH(25℃)
D.水的电离是吸热的过程
参考答案:D
本题解析:
本题难度:一般
5、填空题 (10分,每空2分)某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.0ml于锥形瓶中,加入10.0ml的KI溶液(足量),发生的反应为:Cl2+2KI=2KCl+I2,滴入指示剂2~3滴。
②取一滴定管依次用自来水、蒸馏水洗净后,马上注入0.01mol・L-1Na2S2O3溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3="2NaI+" 2Na2S4O6试回答下列问答:
(1)步骤①加入的指示剂是 。
(2)步骤②应使用 式滴定管。
(3)判断达到滴定终点的实验现象是 ;
(4)氯的实际浓度比所测浓度会偏小,造成误差的原因是
(5)用0.1032mol/L HCl溶液滴定未知浓度的NaOH溶液,下列情况对实验结果无影响的是
A.酸式滴定管未用标准盐酸溶液润洗
B.锥形瓶未用待测液润洗
C.滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了
D.滴定时将标准液溅出锥形瓶外
参考答案:淀粉溶液;碱;滴入最后一滴标准液,溶液由蓝色变成无色且半分钟
本题解析:
试题分析:本滴定实验为利用I2+2Na2S2O3="2NaI+" 2Na2S4O6测定生成I2从而确定水样中的Cl2,故所用指示剂用来指示溶液中I2的量,故应用淀粉溶液作指示剂;步骤②中滴定管所装溶液为Na2S2O3,溶液呈碱性,故应用碱式滴定管;判断达到滴定终点的实验现象是滴入最后一滴标准液,溶液由蓝色变成无色且半分钟内不恢复;步骤②中洗涤滴定管应用水洗后再用Na2S2O3溶液润洗,该步骤没有润洗故会导致所装标准液Na2S2O3溶液浓度变小,故消耗体积变大,故会导致所测水样中Cl2浓度偏大;(5)中依据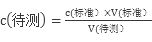 可知A项酸式滴定管未用标准盐酸溶液润洗会导致c(标准)变小,则V(标准)偏大故所测NaOH溶液浓度偏大;锥形瓶不能用待测液润洗,故B项不会产生影响;C项滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了则会导致V(标准)包含气泡体积偏大,故会导致所测浓度偏大;滴定时将标准液溅出锥形瓶外会导致V(标准)偏大故所测NaOH溶液浓度偏大。
可知A项酸式滴定管未用标准盐酸溶液润洗会导致c(标准)变小,则V(标准)偏大故所测NaOH溶液浓度偏大;锥形瓶不能用待测液润洗,故B项不会产生影响;C项滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了则会导致V(标准)包含气泡体积偏大,故会导致所测浓度偏大;滴定时将标准液溅出锥形瓶外会导致V(标准)偏大故所测NaOH溶液浓度偏大。
考点:滴定实验操作。
本题难度:一般