微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N2(g)+3H2(g)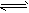 2NH3(g),673 K,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
2NH3(g),673 K,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
下列叙述正确的是
 [???? ]
[???? ]
A.点e的正反应速率比点d的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)相同
D.在给定条件下,t1时刻NH3的含量达到最高
2、填空题 在一定条件下,反应3A(g) + B  ?2C +2D达到平衡
?2C +2D达到平衡
(1)若升高温度,平衡向正反应方向移动,则逆反应是___________(填“吸热”或“放热”)反应,逆反应速率____________(填“增大”或“不变”或“变小”)
(2)若增加或减少B时,平衡不移动,则B是__________态。
(3)若增大压强,平衡向逆反应方向移动,则可判断:B是___态,C是___态,D是__态
3、选择题 在容积相同的A、B两个密闭容器中,分别充入2molSO2和1molO2,使它们在相同温度下发生反应:2SO2+O2 2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
A.25%?????? B.>25%?????? C.<25%??????? D.12.5%
4、计算题 在某温度下,将H2(g)和I2(g)各0.1mol的气体混合物充入10L的密闭容器中,充分反应,达到平衡时,测得c(H2)=0.0080mol/L,
求:
(1)求该反应的平衡常数。(4分)
(2)在上述温度下,该容器中若充入的H2(g)和I2(g)各0.2mol,求达到化学平衡时HI(g)的平衡浓度。(4分)
5、填空题 (12分)现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高。
(1)已知1 mol N2(g)与适量H2(g)完全反应,当生成NH3(g)0.1mol时,放出9.22kJ热量,写出反应的热化学方程式:???????????????????????????????????????。
(2)若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1?????K2(填“>”? “="”" 或 “<” )。
(3)在一定温度下,向容积不变(始终为10L)的密闭容器中加入2 mol N2、8 mol H2 及固体催化剂。10分钟后反应达到平衡状态,容器内气体压强变为起始的80%,此时氨气的体积分数为??????????,用氮气表示的反应速率:??????????????????。若想提高氨气的产率,根据化学平衡移动原理,请提出合理的建议:?????????????????????(任意写一条)。
(4)在上述相同条件下,若起始时加入4 mol NH3、2 mol H2及固体催化剂,反应达到平衡时NH3的体积分数比(3)中??????????(填“大”、“小”或“相等”)。
(5)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如右图)。在电解法合成氨的电解池中???????????????(填“能”或“不能”) 用水作电解质溶液的溶剂,原因是??????????????。
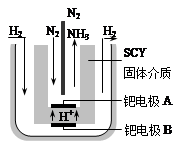
钯电极A是电解池的?????极(填“阳”或“阴”),该极上的电极反应式是????????????????。