微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 《新科学家》2009年1月10日报道,通过取样分析,目前地球大气中二氧化碳的水平是385ppm,带来了明显的温室效应.“ppm”是一种
A.浓度单位
B.质量单位
C.体积单位
D.长度单位
参考答案:A
本题解析:分析:ppm浓度用溶质质量占全部溶液质量的百万分比来表示的浓度,也称百万分比浓度.
解答:ppm浓度用溶质质量占全部溶液质量的百万分比来表示的浓度,也称百万分比浓度,所以“ppm”是一种浓度单位,故选:A.
点评:本题主要考查了ppm浓度的概念,难度不大,掌握概念即可完成.
本题难度:困难
2、选择题 下列各组离子中,能大量共存的一组是
A.K+、NO3-、Na+、CO32-
B.Na+、Cl-、H+、HCO3-
C.Mg2+、Al3+、Cl-、OH-
D.Ca2+、CO32-、K+、OH-
参考答案:A
本题解析:分析:A.根据四种离子相互不会反应进行判断;
B.根据碳酸氢根离子与氢离子反应生成水和二氧化碳进行分析;
C.Mg2+、Al3+与OH-生成沉淀,不能共存;
D.根据碳酸根离子与钙离子生成沉淀进行分析.
解答:A.K+、NO3-、Na+、CO32-四种离子相互交换成分不会生成沉淀或气体或水,不会发生氧化还原反应,可以共存,故A正确;
B.HCO3-与H+两种离子能结合成水和二氧化碳,HCO3-+H+=H2O+CO2↑,不能大量共存,故B错误;
C.Mg2+、Al3+、与Cl-、能共存,但Mg2+、Al3+、与OH-生成沉淀,不能共存,如Mg2++2OH-=Mg(OH)2↓生成沉淀,发生了复分解反应,不能共存,故C错误;
D.碳酸根离子和钙离子反应生成碳酸钙沉淀,Ca2++CO32-=CaCO3↓,不能大量共存,故D错误;
故选A.
点评:本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生氧化还原反应,能否应生成沉淀、气体、水等,题目较简单.
本题难度:困难
3、选择题 将过量的CO2通过Na2O2固体,固体质量增加了28g,则反应的CO2在标准状况下的体积是
A.22.4L
B.11.2L
C.5.6L
D.44.8L
参考答案:A
本题解析:分析:利用差量法,分析Na2O2与CO2反应前后固体质量的变化量,2CO2+2Na2O2=2Na2CO3+O2△m为2Na2CO3-2Na2O2=2CO,可知,反应前后,固体质量增加量为CO的质量,再根据碳守恒,求出CO2的质量,最后求出CO2在标准状况下的体积.
解答:2CO2+2Na2O2=2Na2CO3+O2△m为2Na2CO3-2Na2O2=2CO,可知,反应前后,固体质量增加量为CO的质量,
则n(CO)=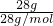 =1mol,
=1mol,
根据根据碳守恒,n(CO2)=n(CO)=1mol,
所以CO2在标准状况下的体积为1mol×22.4L/mol=22.4L,故选:A.
点评:Na2O2与CO2反应的相关计算,复杂而繁琐.但如果能从原理上深刻理解,抓住实质并灵活应用,便可以找到解决问题的捷径.
本题难度:简单
4、选择题 以下物质间的每步转化,不能通过一步反应实现的是
A.S→SO3→H2SO4
B.Al(OH)3→Al2O3→Al
C.Cu→CuCl2→Cu(OH)2
D.Na→Na2O2→Na2CO3
参考答案:A
本题解析:
本题难度:简单
5、选择题 下列离子能大量共存,且满足相应要求的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:A.根据电荷守恒分析;
B.Fe3+遇KSCN,溶液为血红色;
C.离子之间相互促进水解;
D.离子之间不反应,能共存,且加NaOH浓溶液,先发生酸碱中和,再与铵根离子反应.
解答:A.阳离子电荷总数小于阴离子电荷总数,由电荷守恒可知,不能成立,故A错误;
B.Fe3+遇KSCN,溶液为血红色,而不是沉淀,故B错误;
C.Al3+、HCO3-离子之间相互促进水解,不能共存,故C错误;
D.离子之间不反应,能共存,且加NaOH浓溶液,先发生酸碱中和,再与铵根离子反应生成氨气,符合要求,故D正确;
故选D.
点评:本题考查离子的共存,明确习题中的信息及离子之间的反应是解答本题的关键,注意信息中两个要点,选项A为易错点,题目难度不大.
本题难度:困难