微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<
I-<SO2,则下列反应中不能发生的是[???? ]
A.H2O2 + H2SO4 ══ SO2 ↑ + O2 ↑ + 2H2O
B.I2 + SO2 + 2H2O ══ H2SO4 + 2HI
C.2Fe2+ + Cl2 ══ 2Fe3+ + 2Cl-
D.2Fe3+ + SO2 + 2H2O ══ 2Fe2+ + SO42-+ 4H+
参考答案:A
本题解析:
本题难度:一般
2、选择题 常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+="==" 2Fe3++2H2O 2Fe3++H2O2 ="==" 2Fe2++O2↑+2H+
下列说法正确的是
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+弱
B.在H2O2分解过程中,溶液的pH逐渐下降
C.H2O2分解的总方程式为:H2O2===H2O+O2↑
D.H2O2生产过程要严格避免混入Fe2+
参考答案:D
本题解析:
试题分析:A项H2O2的氧化性比Fe3+强,其还原性比Fe2+强,错误;B项这两个反应的总反应为2H2O2=2H2O+ O2↑,水增多,溶液的体积略增大(酸性减弱),溶液的pH略增大,错误;C项H2O2分解的总方程式为:2H2O2===2H2O+O2↑,错误;D项在H2O2生产过程要严格避免混入Fe2+,否则易导致H2O2的分解,正确。
考点:考查化学反应原理等。
本题难度:困难
3、选择题 常温下,下列三个反应均能发生:
X2+2W2+ =2X-+2W3+;
2Z+2X-=2Z-+X2;
2W3++2Y-=2W2++Y2。
则在相同条件下,下列三个反应:
①Y2+2X-=2Y-+X2;
②2Z2+2Y-=2Z-+Y2;
③2W3++2Z-=2W2++Z2
也能发生的是? [???? ]
A.只有①
B.只有②
C.①和②
D.②和③
参考答案:B
本题解析:
本题难度:一般
4、实验题 (13分)已知HI是一种无色,有刺激性气味,极易溶于水的气体,HI的水溶液称之为氢碘酸,是一种强酸。
(1)请写出碘元素在周期表的位置:第五周期 族。
(2)将HI气体通入一定量的浓硫酸中,产生的混合气体除含HI、少量的I2蒸气和水蒸气外,还可能
有 气体。
(3)小明拟对HI通入浓硫酸后的混合气体成分进行验证和探究。他设计了如右实验装置图初步探究设计:
①其中直形玻璃管中所装的药品是 (写名称)
②足量四氯化碳的两个作用是: , 。
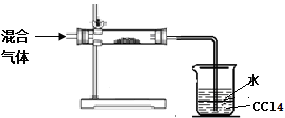
进一步探究:
查阅资料:氧化性强弱KMnO4>HNO3>I2>SO42-,且较稀的硝酸不能氧化I2。
③小明拟对溶在水层的其它混合气体成分做进一步探究。请你从以下限选试剂中选择合适的试剂帮小明完成实验报告。
限选的试剂:石蕊试剂、品红溶液、酸性KMnO4溶液、0.1mol/L HNO3、淀粉溶液、BaCl2溶液
实验方案
| 可能的现象和相应的结论
|
取少量烧杯中的上层溶液分装入A、B两支试管中
|
|
|
|
|
参考答案:(1) VIIA(1分)
本题解析:
试题分析:(1)碘的原子序数是53,因此碘元素在周期表的位置是第五周期第VIIA族。
(2)由于浓硫酸具有氧化性,而碘化氢具有还原性,能被浓硫酸氧化生成单质碘,硫酸被还原为SO2,所以将HI气体通入一定量的浓硫酸中,产生的混合气体除含HI、少量的I2蒸气和水蒸气外,还可能有SO2气体。
(3)①由于气体通过溶液时会带出水蒸气,所以首先检验水蒸气,一般用五水硫酸铜,即其中直形玻璃管中所装的药品是无水硫酸铜。
②碘能被四氯化碳萃取,又因为碘化氢极易溶于水,所以足量四氯化碳的两个作用是检验、吸收碘蒸气和起防倒吸作用。
③由于上层溶液中溶解的是碘化氢和SO2,检验SO2可以用品红溶液。又因为氧化性强弱KMnO4>HNO3>I2>SO42-,且较稀的硝酸不能氧化I2,所以检验碘离子应该用稀硝酸,因此实验方案可设计为
实验方案
可能的现象和相应的结论
往A试管中加入少量品红溶液(1分)
若品红溶液褪色,则原混合气体中有SO2
若溶液不褪色,则原混合气体中没有SO2(1分)
往B试管中滴加足量硝酸溶液后(1分),再滴入少量淀粉溶液(1分)
若淀粉溶液变蓝,则原混合气体中有HI
若溶液不变蓝,则原混合气体中没有HI(1分)
考点:考查物质性质实验方案设计与探究
本题难度:一般
5、选择题 常温下,在溶液中可以发生反应:X+2Y3+=2Y2++X2+,则下列叙述
①X被氧化;②X是氧化剂;③X具有还原性;④Y2+是氧化产物;
⑤Y2+具有还原性;⑥Y3+的氧化性比X2+的氧化性强。
以上叙述中正确的是
A.②④⑥
B.①③④
C.①③⑤⑥
D.②⑤
参考答案:C
本题解析:依据化合价的升降进行判断(升失氧、降得还)即可。
本题难度:一般
|