微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 标准状况下,将V L气体(摩尔质量为M g/mol)溶于0.2L水中,所得溶液的密度是a g/cm3,则此溶液的物质的量浓度(mol/L)为
A.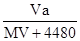
B.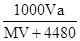
C.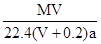
D.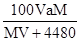
参考答案:B
本题解析:标准状况下,将V L气体的物质的量为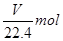 ,其质量为
,其质量为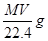 ;所以溶液的质量分数为
;所以溶液的质量分数为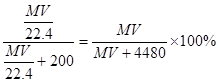 ;根据物质的量的浓度与质量分数的关系可得:
;根据物质的量的浓度与质量分数的关系可得: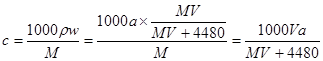 mol/L
mol/L
本题难度:一般
2、计算题 与171 g Al2(SO4)3中所含的SO42-数目相同的Na2SO4的质量是多少?将171 g Al2(SO4)3和142 g Na2SO4混合,其混合物的平均摩尔质量是多少?
参考答案:213g、208.67 g/mol
本题解析:(1)n[Al2(SO4)3]="m/M=171" g÷342 g/mol="0.5" mol
n(SO42-)=3×n[Al2(SO4)3]=3×0.5 mol="1.5" mol
m(Na2SO4)="1.5" mol×142 g/mol="213" g
(2) n[Al2(SO4)3]=" m/M=" 171 g÷342 g/mol="0.5" mol
n(Na2SO4)=" m/M=142" g÷142 g/mol="1" mol
M(平均)= =(171 g+14
本题难度:简单
3、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.在反应5NH4NO3 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA
2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA
B.12.5 mL 16 mol・L-1浓硫酸与足量铜反应,转移电子数为0.2NA
C.标准状况下,1.12L的SO3所含的原子数约为0.2NA
D.标准状况下,2.2gCO2气体中所含分子数为0.05NA
参考答案:D
本题解析:
试题分析:A、每生成4 mol N2,转移电子数为15NA,错误;B、随着反应的进行,浓硫酸渐渐变成稀硫酸
就不再和铜发生反应,所以转移电子数小于0.2NA,错误;C、标准状况下,三氧化硫是固体,错误;D、正确。
本题难度:一般
4、选择题 下图是某品牌饮用矿泉水的标签的部分内容.下列说法正确的是( )
饮用矿物质水
净含量:500mL???配料表:纯净水???硫酸镁???氯化钾??保质期:12个月
主要离子成份:钾离子(K+):1.0~27.3mg/L?镁离子(Mg2+):0.1~4.8mg/L
氯离子(?Cl-):10~27.3mg/L????硫酸根离子(SO42-):0.4~19.2mg/L
A.标签上给出的离子的物理量是离子的物质的量浓度
B.任何饮用水中氯离子(Cl-)的浓度均在10~27.3mg/L
C.该品牌饮用矿泉水中c?Cl-)最大值为10~27.3mg/L之内
D.一瓶该品牌饮用矿泉水中SO42-的物质 的挝不超过1×10-5mol
参考答案:A、该品牌饮用矿物质水中离子浓度表示单位体积内含有离子的质量
本题解析:
本题难度:一般
5、选择题 如图所示:2个甲分子反应生成1个丙分子和3个乙分子,对此下列判断不正确的是

A.化学反应中分子的种类发生了改变
B.该反应类型是分解反应
C.反应生成的丙物质属于单质
D.根据阿伏加德罗定律可推知,1个乙分子中含有2个A原子
参考答案:D
本题解析:
试题分析:已知2个甲分子反应生成1个丙分子和3个乙分子,根据阿伏伽德罗定律和质量守恒定律知1个乙分子中含有2个A原子。D正确。
本题难度:一般
|