微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 实验室使用的浓盐酸的溶质质量分数为36.5%,密度为1.19g?cm3,则物质的量浓度是
A.11.9
B.11.9mol?L-1
C.0.012mol?L-1
D.无法计算
参考答案:B
本题解析:分析:根据c= 计算该浓盐酸的物质的量浓度.
计算该浓盐酸的物质的量浓度.
解答:盐酸的溶质质量分数为36.5%,密度为1.19g?cm3,
则该浓盐酸的物质的量浓度为 mol/L=11.9mol/L.
mol/L=11.9mol/L.
故选:B.
点评:考查物质的量浓度与溶液质量分数的关系,难度中等,可以根据定义法计算,求出溶液的体积是关键.
本题难度:简单
2、选择题 用NA表示阿伏加德罗常数的值.下列说法正确的是
A.1?mol/LCuCl2溶液中含有Cl-的个数为2NA
B.14?g?CnH2n中含有的共用电子对数为NA
C.电解精炼铜时,每转移2?mol电子阳极上溶解的铜原子数为NA
D.标准状况下11.2?L?NH3溶于1?L水中,溶液中含N原子的微粒总数为0.5NA
参考答案:D
本题解析:分析:A、溶液中离子数目与离子浓度、溶液体积有关.
B、根据原子最外层电子数计算每个CnH2n分子中含有共用电子对数为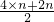 =3n对,根据n=
=3n对,根据n=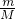 计算14gCnH2n的物质的量,再根据N=nNA计算共用电子对数.
计算14gCnH2n的物质的量,再根据N=nNA计算共用电子对数.
C、电解精炼铜时,阳极放电物质除铜外还有其它物质.
D、根据n=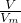 计算氨气的物质的量,根据氮原子守恒可知,溶液中氮原子数目等于11.2LNH3含有的氮原子数目.
计算氨气的物质的量,根据氮原子守恒可知,溶液中氮原子数目等于11.2LNH3含有的氮原子数目.
解答:A、1?mol/LCuCl2溶液中氯离子浓度为2mol/L,液中离子数目与离子浓度、溶液体积有关,溶液体积为告诉,无法计算离子浓度,故A错误;
B、14gCnH2n的物质的量为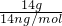 =
=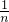 mol,每个CnH2n分子中含有共用电子对为3n对,所以,14gCnH2n中含有的共用电子对数为3NA,故B错误;
mol,每个CnH2n分子中含有共用电子对为3n对,所以,14gCnH2n中含有的共用电子对数为3NA,故B错误;
C、电解精炼铜时,若只有铜放电每转移2mol电子阳极上溶解的铜原子数为NA,阳极放电物质除铜外还有其它物质,所以溶解的铜原子数小于NA,故C错误;
D、标准状况下11.2LNH3的物质的量为0.5mol,根据氮原子守恒可知,溶液中氮原子数目等于11.2LNH3含有的氮原子数目为0.5NA,故D正确.
故选:D.
点评:考查常用化学计量有关计算,难度中等,注意B选项中共用电子对数目的计算.
本题难度:困难
3、选择题 胶体在人们日常生活中随处可见.下列分散系属于胶体的是
A.豆浆
B.矿泉水
C.白醋
D.白酒
参考答案:A
本题解析:分析:胶体的分散质微粒直径在1~100nm之间,是一种均一介稳定的分散系
解答:A、豆浆是蛋白质形成的分散系属于胶体,故A正确;
B、矿泉水四溶液不是胶体,故B错误;
C、白醋是醋酸溶液不是胶体,故C错误;
D、白酒是酒精的水溶液不是胶体,故D错误;
故选A.
点评:本题考查胶体的特点,明确胶体分散质微粒直径在1~100nm之间,是对基础内容的考查,难度不大.
本题难度:困难
4、选择题 设NA表示阿伏加德罗常数的数值,下列叙述中正确的是
A.28g以任意比组成的CO与N2混合气体中含有原子数为2NA
B.标准状况下,22.4LH2O含有的分子数为NA
C.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移4NA个电子
D.1L1mol/L的盐酸中有NA个HCl分子
参考答案:A
本题解析:分析:A.根据n=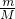 =
=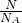 结合分子的组成判断;
结合分子的组成判断;
B.标准状况下,水为液体;
C.根据化合价的变化结合方程式判断;
D.HCl为强电解质,在溶液中电离.
解答:A.CO与N2的相对分子质量都为28,n=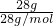 =1mol,都为双原子分子,则28g以任意比组成的CO与N2混合气体中含有原子数为2NA,故A正确;
=1mol,都为双原子分子,则28g以任意比组成的CO与N2混合气体中含有原子数为2NA,故A正确;
B.标准状况下,水为液体,Vm≠22.4L/mol,故B错误;
C.32g氧气为1mol,生成1molO2,转移电子的物质的量为2mol,转移2NA个电子,故C错误;
D.HCl为强电解质,在溶液中电离,不存在HCl分子,故D错误.
故选A.
点评:本题考查阿伏加德罗常数,题目难度不大,本题注意物质的状态以及性质,为易错点.
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值,下列说法正确的是
A.100mL1mol?L-1的Na2S溶液中离子总数为0.3NA
B.2.3gNa在空气中完全燃烧失去0.1NA个电子
C.1mol?C2H4分子中共用电子对数目为5NA
D.标准状况下,44.8?L?CCl4中含2NA个分子
参考答案:B
本题解析:分析:A.根据反应S2-+H2O HS-+OH-判断;
HS-+OH-判断;
B.根据2.3gNa的物质的量和最外层电子数判断;
C.根据乙烯的结构简式CH2=CH2判断;
D.标准状况下CCl4为液体.
解答:A.有反应S2-+H2O HS-+OH-可知,100mL1mol?L-1的Na2S溶液中离子总数大于0.3NA,故A错误;
HS-+OH-可知,100mL1mol?L-1的Na2S溶液中离子总数大于0.3NA,故A错误;
B.2.3gNa为0.1mol,根据Na~Na+~e-可知,2.3gNa在空气中完全燃烧失去0.1NA个电子,故B正确;
C.由乙烯的结构简式CH2=CH2可知,C和4个H形成4个共价键,有4个共用电子对,并且C=C键有2个共用电子对,共有6个共用电子对,故C错误;
D.标准状况下CCl4为液体,Vm≠22.4L/mol,故D错误.
故选B.
点评:本题考查阿伏加德罗常数,题目难度不大,易错点为A,注意物质的性质.
本题难度:困难