��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ˮ�ڿ����г��ڷ��ã�������ˮ����������£������������ʵ�����������ǣ�������
A��ClO-
B��HClO
C��ˮ
D��Cl-
2������� ��������Դ�ı��⣬�̲��ŷḻ�Ļ�ѧԪ�أ����ȡ��塢��ȡ�
(1)�ڹ��������£�������������Ӧ�������£�
��Cl2�D��Cl��Cl����Cl��H2�D��HCl��H����H��Cl2�D��HCl��Cl ����
��Ӧ�����γɵĻ�����ĵ���ʽΪ______����Ӧ���б��ƻ��Ļ�ѧ������______��(����ԡ��Ǽ��ԡ�)��
(2)�ڶ���������Ԫ���У���Ԫ�ؼ���������Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳����________???????(��Ԫ�ط��ű�ʾ)������Ԫ��ͬ�����ҽ�������ǿ��Ԫ��λ�����ڱ��ĵ�________����________�塣
(3)±�ص��ʼ������������������϶������ŵݱ���ɡ������й�˵����ȷ����____��
a��±��������ɫ��AgCl��AgBr��AgI��˳�����μ���
b��±����ļ�����H��F��H��Cl��H��Br��H��I��˳�����μ�С
c��±����Ļ�ԭ��HF��HCl��HBr��HI��˳�����μ���
d��±�ص������������ϰ�F2��Cl2��Br2��I2��˳�����ѱ���
(4)±�ص��ʵļ��ܴ�С��ͼ����ͼ�ƶϣ�

�ٷǽ�����ǿ��±�أ��䵥�ʷ��ӵĻ�ѧ��________����(����ס������ס���һ�����ס�)��
��±�ص��ʼ��ܴ�С������Ĺ�ϵΪ��______________________________________��
3��ʵ���� �����������������ѧ��ѧ�еij������壬̽�����ߵ��Ʒ���������ʮ����Ҫ�Ŀ��⡣
��1��ʵ���ҿ��ɶ���;����ȡSO2��
;��I��Na2SO3�������Ũ�����ᣨԼ70%����Ӧ��ȡ��
;��II��ͭ��Ũ���������ȡ��
���Ҫ��ʵ������ȡSO2��ѡ���������ַ����е�????????���;��I����;��II���������������������????????????????????????(���һ��Ϳ�)��
��2����ͼ����KMnO4��Ũ���ᷴӦ��ȡ���������ļ���װ�á�
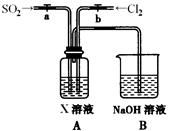
��֪��2 KMnO4+16HCl��Ũ��= 2KCl+2MnCl2+5Cl2��+8H2O��װ��B��C��D�����÷ֱ��ǣ�
B��???????????????????????????��
C��???????????????????????????��
D��???????????????????????????��
��3��ijͬѧ���������װ��̽���������������Ļ�ѧ���ʡ�

ͨ�����Ƶ��ɼ�a��b����װ��A�зֱ�ͨ�벻ͬ���壬������������⣺
�����ر�b����a����XΪƷ����Һ����A�е�����Ϊ��?????????��˵�������������???????????�ԡ�
�����ر�a����b����XΪ��ɫʯ����Һ����A�е�����Ϊ��??????????????????��ԭ����?????????????��
����ͬʱ��a��b����ͨ������������Ϊ1:1����XΪ��ɫʯ����Һ����A�е�����Ϊ????????????????���������ͬ��ԭ����??????????????????????����д��Ӧ�Ļ�ѧ����ʽ����
4������� ij�о���ѧ��С��������ϵ�֪��Ư����������Һ��Ӧ����ȡ��������ѧ����ʽΪ��Ca��ClO��2+CaCl2+2H2SO4
??��??
.
?
2CaSO4+2Cl2��+2H2O�����������ͼ��ʾװ����ȡ��������֤�����ʵ�ʵ�飮
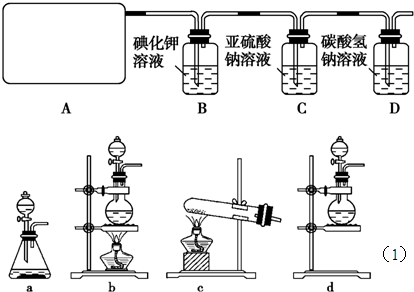
�Իش�
��1����ʵ����A���ֵ�װ����?����дװ�õ���ţ���
��2��B�з�Ӧ�Ļ�ѧ����ʽ��?��
��3��д��C�з�Ӧ�����ӷ���ʽ?����������С��ͬѧ���һ��ʵ�飬֤��ϴ��ƿC�е�Na2SO3�ѱ�����������ʵ�鲽�裩��?��
��4��д����Dװ���з�����Ӧ�����ӷ���ʽ?��
��5����ʵ��������Ե�ȱ����?��
��6����С���ֽ���������ʵ�飺��ȡƯ��2.0g����ĥ���ܽ⣬���Ƴ�250mL��Һ�����������KI��Һ������H2SO4��Һ�����ã�����ȫ��Ӧ����0.1mol?L-1��Na2S2O3��Һ������Һ�ζ���Ӧ���ɵĵ⣬��֪��ӦʽΪ2Na2S2O3+I2�TNa2S4O6+2NaI����Ӧ���ʱ��������Na2S2O3?200mL�����Ư����Ca��ClO��2����������Ϊ?��
5��ѡ���� �����������ж����д̼�����ζ������ɫ�������ǣ�???��
A��H2S
B��NH3
C��NO2
D��SO2
|