微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据金属活动性顺序表,Cu不能发生:Cu+2H2O=Cu(OH)2+H↑的反应.但选择恰当电极材料和电解液进行电解,这个反应就能变为现实.下列四组电极和电解液中,能实现该反应最为恰当的是( )
| 阳极 | 阴极 | 电解液
A
石墨棒
石墨棒
CuSO4溶液
B
Cu
石墨棒
Na2SO4溶液
C
Cu
Fe
H2SO4溶液
D
Cu
Pt
H2O
A.A
B.B
C.C
D.D
参考答案:A、选项是电解硫酸铜溶液,阳极上氢氧根离子失电子发生氧化反应
本题解析:
本题难度:一般
2、选择题 从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、在HCl气体氛围中干燥产物;④将得到的产物熔融电解得到镁。下列说法不正确的是
A.①②③步骤的目的是从海水中获得MgCl2
B.以上提取镁的过程中涉及化合、分解和复分解等反应
C.第④步电解时阳极产生氯气
D.第④步电解时阴极与阳极产物的物质的量之比为1:2
参考答案:D
本题解析:
试题分析:把贝壳制成石灰乳涉及两步反应,首先贝壳高温分解制成氧化钙,然后氧化钙与水结合制成石灰乳;在引入的海水中加石灰乳后,石灰乳的主要成分氢氧化钙与海水中的镁离子结合生成氢氧化镁沉淀;氢氧化镁与盐酸反应生成氯化镁;电解熔融的氯化镁得到金属镁。分析上述转化过程,可知反应中没有涉及置换反应,所以选项D不正确,其余选项D都是正确的,答案选D。
本题难度:一般
3、选择题 常温时,将500 mL pH=5的CuSO4溶液用石墨电极电解一段时间,测得溶液的pH变为2,若使溶液的浓度、pH与电解前相同,可采用的方法(??)。
A.向溶液中加入0.245g Cu(OH)2
B.向溶液中加0.31g CuSO4
C.向溶液中加0.0025 mol H2SO4并加热
D.向溶液中加0.2g CuO
参考答案:D
本题解析:加入的物质与电解过程中溶液失去的物质的组成应该完全相同。电解CuSO4溶液时放电的离子为Cu2+和O2,因此应该加入的物质中只含有Cu和O两种元素。该题目不必要计算即可判断。?
本题难度:一般
4、选择题 电解质量分数为0.052(5.2%)的NaOH溶液1 L(密度为1.06 g/cm3),用铂作电极电解,当溶液中NaOH的质量分数改变了0.010(1.0%)时停止电解,此时溶液中符合下表关系的是 [???? ]
NaOH的质量分数?
阳极析出物质的质量/g
?阴极析出物质的质量/g
A.
0.062(6.2%)
19
?152
B.
0.062(6.2%)
?152
19
C.
0.042(4.2%)?
1.2
9.4
D.
0.042(4.2%)?
9.4
?1.2
参考答案:B
本题解析:
本题难度:一般
5、填空题 (14分)亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3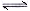 H++ H2PO3-。亚磷酸与足量NaOH溶液反应,生和Na2HPO3。 H++ H2PO3-。亚磷酸与足量NaOH溶液反应,生和Na2HPO3。
(1)①写出亚磷酸与少量NaOH溶液反应的离子方程式 。
②根据亚磷酸(H3PO3)的性质可推测Na2HPO3稀溶液的pH 7(填“>”、“<”或“=”)。
③某温度下,0.1000 mol・L-1的H3PO3溶液中c (H+)=2.5×10-2mol・L-1,除OH―之外其他离子的浓度由大到小的顺序是 ,该温度下H3PO3电离平衡的平衡常数K= 。(H3PO3第二步电离忽略不计,结果保留两位有效数字)
(2)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式 。
(3)电解Na2HPO3溶液也可得到亚磷酸,装置示意图如下:
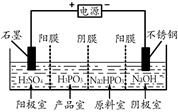
说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过。
①阴极的电极反应式为 。
②产品室中生成亚磷酸的离子方程式为 。
参考答案:(1)①H3PO3+OH―=H2PO3―+H2O
本题解析:
试题分析:(1)①亚磷酸是二元弱酸,与少量NaOH溶液反应生成酸式盐,反应的离子方程式为H3PO3+OH―=H2PO3―+H2O。
②亚磷酸是二元弱酸,因此相应的正盐Na2HPO3在溶液中水解溶液显碱性,则pH>7。
③亚磷酸是二元弱酸,以第一步电离为主,又因为水中还存在电离平衡,所以除OH―之外其他离子的浓度由大到小的顺序是c(H+)> c(H2PO3-)> c(HPO32-);根据H3PO3溶液存在电离平衡H3PO3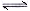 H++ H2PO3-可知,溶液中c(H2PO3-)≈c(H+)=2.5×10-2mol・L-1,c(H3PO3)=0.1000 mol・L-1-2.5×10-2mol・L-1=0.075mol/L,所以该温度下电离常数K= H++ H2PO3-可知,溶液中c(H2PO3-)≈c(H+)=2.5×10-2mol・L-1,c(H3PO3)=0.1000 mol・L-1-2.5×10-2mol・L-1=0.075mol/L,所以该温度下电离常数K=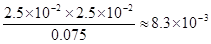 。 。
(2)亚磷酸具有强还原性,可使碘水褪色,在反应中被氧化为磷酸,反应的化学方程式为H3PO3+ I2+H2O = 2HI+ H3PO4。
(3)①电解池中阴极得到电子,因此阴极是溶液中的氢离子放电,电极反应式为2H++ 2e-=H2↑。
②阳极氢氧根离子放电,同时产生氢离子,氢离子进入产品室与Na2HPO3反应得到亚磷酸,所以在产品室生成亚磷酸的方程式为HPO32-+ 2H+=H3PO3。
考点:考查弱电解质的电离、离子浓度大小比较、氧化还原反应以及电化学原理的应用
本题难度:困难
|