微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (17分)
(1)右图所示是实验室中制取气体的一种简易装置。

①请简述检验它的气密性的方法???????????????。
②利用右图所示装置可以制取??????气体(填反应物状况及发生反应是否需要的条件)。
(2)张明同学设计下图所示装置,用粗铁粒与189g・L-1硝酸反应制取NO气体。请回答有关问题。

①189g・L-1硝酸的物质的量浓度为????????。
②NO气体能用排水法收集,而不能用排空气法收集的可能原因是?????????。
③当找末止水夹a,关闭止水夹b时,A装置的干燥管中观察到的现象是???????。B装置烧杯中液体的作用是????????????。当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体。
④该实验中,若去掉B装置,对实验结果是否有影响??????????????。
⑤将a mol铁与含b molHNO3的稀溶液充分反应后,若HNO3的还原产物只有NO,反应后Fe和HNO3均无剩余,则反应中转移电子的物质的量是?????(用含a和b的代数式表示)。
⑥完全反应后,A装置烧杯里含铁的价态可能是????????。现有仪器和药品:试管和胶头滴管。0.1mol・L-1KSCN溶液、0.1mol・L-1KI溶液、0.2mol・L-1酸性KMnO4溶液、氯水等。请你设计一个简单实验,探究上述判断,填写下列实验报告:
实验步骤
| 操作
| 现象与结论
|
第一步
| 取少量液体装于试管,向试管中滴入几滴KSCN溶液
| ?
|
第二步
| ?
| 若溶液紫色退去,则说明含有Fe2+,若无明显变化,则说明不含Fe2+
2、填空题 (14分)某学生实验小组拟用孔雀石(主要成分是Cu(OH)2・CuC03,其杂质主要为FeC03等)制胆矾,实验设计流程如下:

回答下列问题:
(1)步骤(a)中,实验研磨孔雀石的仪器名称??????????;用硫酸浸取的化学方程式:??????????????????????
(2)步骤(b)中,pH控制在3.O~3.5,其目的是????????????????????????;加过氧化氢发生反应的离子方程式为???????????????????????????????????????????????。
(3)怎样判断蒸发浓缩已完成:??????????????????????????????????????????。
(4)将制得的样品用热重仪进行热重分析,热重仪原理及热重记录如下表:
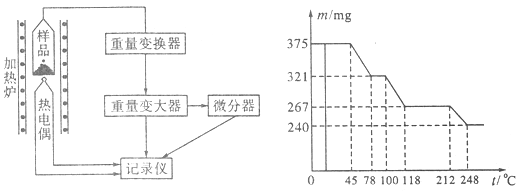
写出212~248℃温度范围内发生反应的化学方程式??????????????????????????????。
(5) FeC03为白色沉淀,此沉淀的Ksp(FeC03)=2×10-11,将FeCl2的稀溶液与Na2CO3溶液等体积混合,若FeCl2的浓度为2×lO一5mol・L-1.则生成沉淀所需Na2CO3溶液的最小浓度为????mol・L-1。
3、实验题 1,2,3,4―四氢化萘的结构简式如下图, 分子式是C10H12。常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+ 4Br2→ C10H8Br4+ 4HBr生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:

①按一定质量比把四氢化萘和水加入适当的容器中,加入少量纯铁粉。
②慢慢滴入液溴,不断搅拌,直到反应完全。
③取下反应容器,补充少量四氢化萘,直到溶液颜色消失。过滤,将滤液倒入分液漏斗,静置。
④ 分液,得到的“水层”即氢溴酸溶液。
回答下列问题:
(1) 如图所示的装置, 适合步骤①和②的操作的是????????????????????????。
(2) 步骤②中如何判断“反应完全”_________________________________________。
(3) 步骤③中补充少量四氢化萘的目的是??????????????????????????????????。??
(4) 步骤③中过滤后得到的固体物质是____________??????????????_________。
(5) 已知在实验条件下,饱和氢溴酸溶液中氢溴酸的质量分数是66%,如果溴化反应进行完全,则步骤①中水和四氢化萘的质量比约是1:____________(保留小数点后1位)。
4、实验题 .(12分)在实验室中用二氧化锰跟浓盐酸反应制备干燥且较纯净的氯气。进行此实验,所用仪器如下图:

(1)连接上述仪器的正确顺序是(填各接口处的字母):
????接????,_____接????,_____接????,????接????。
(2)在装置中:
①饱和食盐水的作用是???????????????????????????????,
②浓硫酸的作用是???????????????????????????????????????。
(3)写出下列化学反应的化学方程式:
①气体发生装置中进行的反应:????????????????????????????????;
②尾气吸收装置中进行的反应:????????????????????????????????。
(4)MnO2是______色的粉末状固体,在该实验中MnO2所起得作用是____________
(5)若实验操作正确,在集气瓶内若放一块干燥的有色布条,在实验进行的过程中,有色布条能否褪色?(填“能”或“不能”)________.
5、填空题 下图表示某种盐C的制备及其性质的实验步骤:
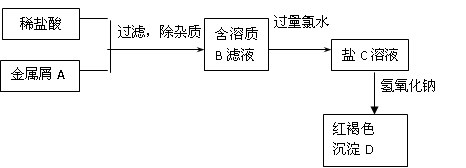 ??? ???
已知:盐C溶液呈黄色;沉淀D焙烧分解,生成红棕色粉末E。
(1)请写出下列物质的化学式:
A?????????,B???????????,C?????????????,D????????????,
(2)写出相应反应的离子方程式
A→B:?????????????????,B→C:????????????????????,
(3)向B的溶液中滴加NaOH溶液,可观察到白色沉淀产生,该沉淀在空气中放置的现象为???????????????????????,发生上述变化的化学方程式为?????????????????????
|