微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 为了测定一置于空气中的某硫酸酸化的FeSO4溶液中Fe2+被氧化的百分率,某同学准确量取pH=1(忽略Fe2+、Fe3+的水解)的FeSO4溶液200 mL,加入过量BaCl2溶液,充分反应后过滤、洗涤、干燥,得到沉淀28.0 g;再另取同样的FeSO4溶液200 mL,向其中加入过量NaOH溶液,搅拌使其充分反应,待沉淀全部变为红褐色后,过滤、洗涤并灼烧所得固体,最终得固体8.0 g。
(1)通过计算,填写下表:
c(H+)
| c(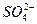 ) )
| c(Fe2+、Fe3+)
|
?
| ?
| ?
注:c(Fe2+、Fe3+)表示Fe2+和Fe3+的总的物质的量的浓度。
(2)计算原溶液中Fe2+被氧化的百分率。
(3)当Fe2+部分被氧化时,试推导c(Fe2+、Fe3+)与c(H+)、c(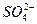 )的关系。 )的关系。
参考答案:(1)0.1 mol・L-1?? 0.6 mol・L-1?
本题解析:(1)由pH=1得c(H+)="0.1" mol・L-1
由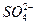 +Ba2+====BaSO4↓得 +Ba2+====BaSO4↓得
c(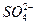 )= )=
本题难度:简单
2、选择题 制印刷电路时常用氯化铁溶液作为“腐蚀液”:发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
[???? ]
A.烧杯中有铜无铁
B.烧杯中有铁无铜
C.烧杯中铁、铜都有
D.烧杯中铁、铜都无
参考答案:B
本题解析:
本题难度:一般
3、填空题 钢铁工业是国家工业的基础,请回答:钢铁冶炼、腐蚀与防护过程中的有关问题。
(1)工业用热还原法冶炼生铁的主要原料有???????????????????????,设备的名称是??????????????????写出用还原剂CO还原赤铁矿(主要成分为Fe2O3)的化学方程式
???????????????????????????????????????????。
(2)写出钢铁在潮湿空气中发生锈蚀时的正极反应方程式??????????????????????????????
生成铁锈(Fe2O3..XH2O)的化学方程式为??????????????????????.
(3)生铁的用途远远不及钢材广泛,人们把较多的高炉生铁直接冶炼成钢,由生铁直接在纯氧顶吹转炉中转化成钢时,是把有害杂质除掉而保留有益元素,可以概括为???????????????????????????????????
??????????????????????????????????????????。为了防止钢铁制品发生锈蚀,可以在钢铁零件的表面进行电镀铜等措施,电镀铜时的阳极反应为??????????????????????????????。
参考答案:(1)铁矿石、焦炭、石灰石???高炉?
Fe2O3+3
本题解析:略
本题难度:一般
4、实验题 合肥市某校化学兴趣小组为探究铁与浓硫酸反应,设计了如图所示装置进行实验。
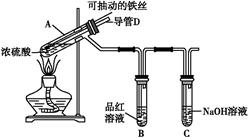
(1)实验过程中,观察到B中的实验现象是???????????????????????????????????????????????? 。
一段时间后,观察到从C中有少量的气泡冒出,此气泡的成分是 ?????????????。
(2)用“可抽动的铁丝”代替“直接投入铁片”的优点是?????????????????????????????????????????????????????????????? ;
反应结束后,不需要打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是????????????????????????????????? 。
(3)反应一段时间后,他们对A中溶液的金属阳离子进行了探究。
①提出假设:
假设1:溶液中只存在Fe2+;
假设2: ??????????????????????????????????;?
假设3:溶液中存在Fe2+和Fe3+。
②请你设计实验验证上述假设1,写出实验操作步骤、实验现象及结论。限选试剂:酸性KMnO4溶液、NaOH溶液、淀粉KI溶液、KSCN溶液。
实验操作步骤
| 实验现象
| 结论
| ?
| ?
| ?
?
参考答案:(1)品红溶液褪色 H2
(2)便于控制铁与浓硫酸的反
本题解析:(1)A中开始可能发生的反应有:2Fe+6H2SO4(浓) Fe2(SO4)3+3SO2↑+6H2O、Fe+Fe2(SO4)3 Fe2(SO4)3+3SO2↑+6H2O、Fe+Fe2(SO4)3 本题难度:一般 本题难度:一般
5、填空题 为测定该补血剂样品[主要成分是硫酸亚铁晶体(FeSO4?7H2O)]中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一:用酸性KMnO4溶液滴定测定铁元素的含量
(1)写出滴定反应的离子方程式______.
(2)下列滴定方式中,最合理的是______(夹持部分略去)(填字母序号).
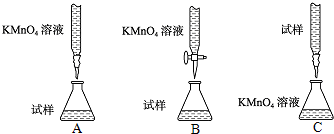
(3)实验前,首先要准确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需______(填仪器名称).
(4)某同学设计以原电池的形式实现Fe2+至Fe3+的转化,电解质溶液为稀硫酸,请写出负极的电极反应式______
方案二?将FeSO4转化为Fe2O3,测定质量变化操作流程如下:
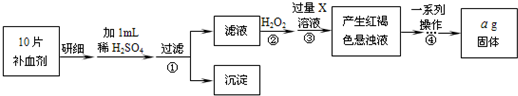
(3)步骤②中除用H2O2外还可以使用的物质是______.
(5)步骤②是否可以省略______,理由是______.
(6)步骤④中一系列操作依次是:过滤、洗涤、______、冷却、称量.
(7)假设实验无损耗,则每片补血剂含铁元素的质量______g(用含a的代数式表示).
参考答案:方案一:(1)酸性高锰酸钾具有强氧化性,将Fe2+氧化为Fe
本题解析:
本题难度:一般
|
|