微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是
A.SO2能使品红溶液褪色是因为SO2具有氧化性,所以它也能使酸碱指示剂褪色
B.硫化氢中硫显最低价态-2价,因此只具有还原性
C.浓硫酸使木棒或棉花变黑,体现了浓硫酸的吸水性
D.BaSO4可作“钡餐”进行X射线检查
2、填空题 Na2S2O3・5H2O 俗称“海波”,是常用的脱氧剂、定影剂和还原剂;它是无色易溶于水的晶体,不溶于乙醇,在20 ℃ 和70 ℃ 时的溶解度分别为60.0 g和212 g,Na2S2O3・5H2O于40~45 ℃熔化,48 ℃分解。下面是实验室制备及相关性质实验。
制备海波的反应原理:Na2SO3+S Na2S2O3
Na2S2O3
制备海波的流程:
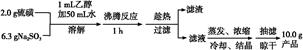
(1)实验开始时用1 mL乙醇润湿硫粉的作用是 。
A.有利于亚硫酸钠与硫磺的充分接触
B.防止亚硫酸钠溶解
C.控制溶液的pH
D.提高产品的纯度
(2)趁热过滤的原因是???????????????????????????????????????????? 。
(3)滤液不采用直接蒸发结晶的可能原因是??????????????????????????????? 。
(4)抽滤过程中需要洗涤产品晶体,下列液体最适合的是 。
A.无水乙醇?????? B.饱和NaCl溶液?????? C.水????? D.滤液
(5)产品的纯度测定:取所得产品10.0 g,配成500 mL溶液,再从中取出25 mL溶液于锥形瓶中,滴加几滴淀粉作指示剂,然后用0.050 mol/L的标准碘水溶液滴定,重复三次,平均消耗20 mL标准碘水,涉及的滴定反应方程式为:I2+2Na2S2O3 2NaI+Na2S4O6。产品中的Na2S2O3・5H2O的纯度为 %。
2NaI+Na2S4O6。产品中的Na2S2O3・5H2O的纯度为 %。
3、选择题 下列化合物:①SO3 ②Fe(OH)3 ③FeCl2 ④CuS ⑤H2SiO3 ⑥NaHCO3其中不可能通过化合反应制得的是 [???? ]
A.①②⑤⑥
B.③④⑤⑥
C.④⑤
D.①②③⑤
4、选择题 已知:FeSO4・7H2O)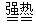 Fe2O3+SO2↑+ SO3↑+ 14H2O,将生成的气体通入BaCl2溶液中,下列叙述中正确的是
Fe2O3+SO2↑+ SO3↑+ 14H2O,将生成的气体通入BaCl2溶液中,下列叙述中正确的是
A.有BaSO4生成
B.有BaSO3生成
C.同时有BaSO4和BaSO3生成
D.有SO3逸出
5、实验题 由下列仪器组成的一套制取SO2并验证它有氧化性、还原性和漂白性。(图中铁架台、铁夹等省略,装置③中E管气体向上流出)②④⑤装置中所用试剂只能从以下物质中选用:氯水、浓H2SO4、溴水、硝酸、品红溶液、烧碱溶液、石灰水。
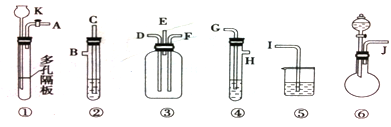
试回答:
(1)连接仪器时,导气管连接顺序从左到右J接_____、_____接_____、H接D、______接I、______接______。
(2)装置②用以检验SO2的还原性,所盛试剂最好是______,装置④中所盛试剂最好是______,装置⑤中所盛试剂最好是_______,目的是??????????????????????????????
(3)仪器连接好后,怎样检查装置①的气密性,简述操作要点???????????????????????????。
(4)书写①装置中反应的化学方程式????????????????????????????????????????????。
书写③装置中反应的化学方程式???????????????????????????????????????????????。