微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 只用一种试剂就能鉴别Ba(NO3)2、Na2CO3、K2SO4三种溶液,该试剂是( )
A.KNO3溶液
B.稀H2SO4
C.NaOH溶液
D.Na2SO4溶液
2、实验题 (16分)某化学研究性小组同学提出回收含铜电缆废料中提取铜的两种方案,并向老师咨询,老师就以下几个方面与同学们展开讨论:
方案甲:

(1)两个方案哪个符合当前生产的绿色理念,为什么?
??????????????????????????????????????????????????????????????????.
(2)写出方案甲中的②③步骤与铜有关的离子反应的离子方程式。
??????????????????????? ??????__________________ _?????? __________
??????__________________ _?????? __________
??????????????????????????????? _________________?????? _________。
(3)老师建议,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑,目的是:???????????????????????????????????。
(4)老师请同学们用化学方法检验红色粉末中是否含有过量的铁屑。请你填写下 列表格写出实验操作、预期实验现象、结论及操作(②中相关的离子方程式)。
序号
| 实验操作
| 实验现象
| 结论及离子方程式
|
①
| 取适量的样品于试管内
| ――
| ――
|
②
| 用滴管滴入足量硫酸溶液,并充分振荡试管
| ?
| ?
|
③
| ?
| 溶液先黄色,滴入KSCN溶液后显红色
| ?
|
?
| ?
| ?
| ?
(5)为了提高原料的,老师建议把最后一步所得浅绿色滤液通过蒸发.冷却结晶.过滤.洗涤.自然干燥得到一种带结晶水的硫酸亚铁晶体。
研究小组按老 师的建议完成上面操作步骤,获得晶体后对其进行检测 师的建议完成上面操作步骤,获得晶体后对其进行检测
①先取a g的晶体进行脱水实验,获得无水固体为(a―1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。研究小组通过计算测知该晶体的化学式是??????????????。
3、实验题 (14分)Fe(OH)2由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用右图装置使用Fe,H2SO4(稀),NaOH溶液可在还原性气氛中制取Fe(OH)2白色沉淀,且较长时间内不变色,其中C为弹簧夹。(提示:还原性气氛如氢气环境)
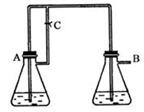
(1)则锥形瓶A中应加入的药品为_________________.(2分)
(2)锥形瓶B中应加入的药品为__________________.(2分)
(3)容器A中的反应开始后,请简单写出完成制备Fe(OH)2的后续操作步骤。
①_____________________?②_______________________________。(4分)
(4)若在反应开始之前先关闭弹簧夹C,则实验现象为:??????????????????????
????????????????????????????????????????????????????????;(2分)
请写出此时B瓶中发生的化学反应的离子方程式:?????????????????????????????
??????????????????????????????????????????????;(4分)
4、实验题 镍电池由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境 有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:

已知:
①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如下表所示:

回答下列问题:
(1)根据上表数据判断步骤②依次析出沉淀Ⅱ:____和沉淀Ⅱ:____(填化 学式),则pH1____pH2(填“>”、“=”或“<”)。
(2)已知溶解度:NiC2O4>NiC2O4・H2O> NiC2O4・2H2O,则步骤③中反应的化学方程式是_______。第③步反应后,过滤沉淀I所需的玻璃仪器有___。
(3)步骤④中阳极反应产生的气体E为一黄绿色气体,写出步骤⑥中反应的离子方程式___
(4) FeCl3和AlCl3的混合溶液中加入NaOH溶液,若Fe(OH)3和Al(OH)3同时存在,则 c(Fe3+)/c(Al3+)=____。
5、实验题 (12分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4++6HCHO??3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容、充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积________(填“偏大”“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察________。
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由________色变成______色。
(2)滴定结果如下表所示:
滴定次数??????待测溶液的体积/mL????标准溶液的体积/mL
滴定前刻度???滴定后刻度
1???? 25.00????? 1.02 21.03
2???? 25.00????? 2.00 21.99
3???? 25.00????? 0.20 20.20
若NaOH标准溶液的浓度为0.101 0 mol・L-1,则该样品中氮的质量分数为________。
|