22
(5)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如下表:
根据表中数据分析:
①温度升高,该反应的平衡常数K值???????(选填“增大”、“减小”或“不变”);
②提高氢碳n(H2)/n(CO2)比,对生成乙醇??????(选填“不利”、“有利”或“无影响”)。
参考答案:(1)CO2+CO32-+H2O==2HCO3-?(3分)<
本题解析:略
本题难度:简单
2、选择题 煤气化的一种方法是在气化炉中给煤炭加氢,发生的主要反应为:C(s)+2H2(g) CH4(g)。在VL的容器中投入a mol碳(足量),同时通入2a molH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压力及温度的变化关系如图所示。下列说法正确的是 CH4(g)。在VL的容器中投入a mol碳(足量),同时通入2a molH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压力及温度的变化关系如图所示。下列说法正确的是
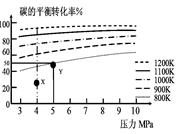
A.上述正反应为吸热反应
B.在4MPa、1200K时,图中X点υ(H2)正 >υ(H2)逆
C.在5MPa、800K时,该反应的平衡常数为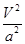 L2・mol-2 L2・mol-2
D.工业上维持6MPa 1000K而不采用10MPa1000K,主要是因
为前者碳的转化率高
参考答案:AB
本题解析:
试题分析:A、由图观察,温度越高碳的平衡转化率越大,平衡正向移动,正反应为吸热反应,正确;B、X点是未平衡时,反应正向进行,正反应速率大于逆反应速率,正确;
C、此时碳转化率为50%
C(s)+2H2(g) CH4(g) CH4(g)
始量?? a???? 2a
转化量0.5a?? a?????? 0.5a
平衡量0.5a?? a?????? 0.5a
k="(0.5a/V)/" ( a/V)2=0.5V/a,错误;
D、该选择的原因是两者转化率相差不大,但压强增大对设备要求高,能量需求大,错误。
本题难度:一般
3、选择题 可逆反应2SO2+O2 2SO3达到平衡的标志是( )。 2SO3达到平衡的标志是( )。
①消耗2 mol SO2的同时生成2 mol SO3 ②SO2、O2与SO3的物质的量之比为2∶1∶2 ③反应混合物中,SO3的质量分数不再改变
A.①②
B.①③
C.③
D.①
参考答案:C
本题解析:①只提到正反应速率;②各物质的物质的量之比为2∶1∶2,若为瞬时,不一定平衡,如保持不变,则平衡;③SO3的质量分数不再改变,即说明各物质浓度不再改变,反应达到平衡。
本题难度:简单
4、选择题 在一个固定容积的密闭容器中发生如下反应:N2 (g) + 3H2 (g) 2NH3 (g)??ΔH =-92.2 kJ/mol在不同时间段里化学反应速率随时间变化如图所示,据此判断下列说法正确的是 2NH3 (g)??ΔH =-92.2 kJ/mol在不同时间段里化学反应速率随时间变化如图所示,据此判断下列说法正确的是

A.处于平衡状态的只有t1~t2段
B.t1~t2段c(NH3)最大
C.在t2时可能是向容器中充入了少量He
D.在t4时可能是升高温度
参考答案:B
本题解析:只要正逆反应速率相等,反应就处于化学平衡状态,所以t1~t2段、t3~t4段、t4~t5段均处于平衡状态,A不正确。根据图像可知t2时反应向逆反应方向移动,所以改变的条件是升高温度,因此选项B正确,C不正确。t4是反应速率增大,但平衡不移动,所以改变的体积是加入了催化剂,D不正确。答案选B。
本题难度:一般
5、选择题 对于N2(g)+3H2(g)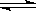 2NH3(g),不能作为反应达到平衡状态的判断依据是(???) 2NH3(g),不能作为反应达到平衡状态的判断依据是(???)
A.单位时间内生成1molN2,同时消耗3molH2
B.恒容密闭容器中总压强不变
C.生成氨气的速率与氨气分解的速率相等
D.N2、H2、NH3的浓度不再发生变化
参考答案:B
本题解析:
试题分析:可逆反应达到化学平衡状态的标志是正、逆反应速率相等、各组分浓度保持不变。单位时间内生成1molN2,为逆反应,同时消耗3molH2,为正反应,且v(正)=v(逆),A是平衡状态;反应正向进行时气体物质的量减小,定温、恒容密闭容器中气体的压强减小,所以压强不变不能说明反应达到平衡状态,需加定温条件,B错误;生成氨气的速率与氨气分解的速率相等即v(正)=v(逆),C是平衡状态;各组分浓度保持不变,说明反应达到平衡状态,D正确。
点评:理解化学平衡状态的直接标志(正、逆反应速率相等、各组分浓度保持不变)和间接标志(体系的压强、温度、颜色、平均摩尔质量等),但一定要分析清楚。
本题难度:一般
|