微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 已知2SO2(g)+ O2(g) 2SO3(g) △H<0 ,温度一定,体积为3L的密闭容器中,投入2 mol SO2和1 molO2, 2min反应达平衡时,容器中有1.2 mol SO3,放出热量117.6 kJ,试计算:
2SO3(g) △H<0 ,温度一定,体积为3L的密闭容器中,投入2 mol SO2和1 molO2, 2min反应达平衡时,容器中有1.2 mol SO3,放出热量117.6 kJ,试计算:
(1)写出该反应的热化学方程式。??
(2)该反应中SO2的转化率是多少?
(3)其他条件相同,若起始时改为充入2 mol SO3,,计算达平衡后SO3的质量分数为多少?
2、选择题 如图表示外界条件(温度、压力)的变化对下列反应的影响:L(s)+G(g) 2R(g)?ΔH>0。在图中Y轴是指
2R(g)?ΔH>0。在图中Y轴是指

A.平衡混合气中R的质量分数
B.G的转化率
C.平衡混合气中G的体积分数
D.L的转化率
3、选择题 反应:A + 3B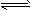 2C + D,在四种不同情况下的反应速率分别为:
2C + D,在四种不同情况下的反应速率分别为:
① ②
②
③ ④
④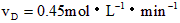
该反应进行得最快的是 [???? ]
A.①
B.④
C.①④
D.②③
4、选择题 反应4A(s)+3B(g)? = 2C(g)+D(s),经2min,B的浓度减少0.6 mol/L。对此反应速率的表示不正确的是?
[???? ]
A.在2 min内的反应速率用B表示为0.3 mol/(L・min)
B.在2 min内用C表示反应速率是0.2 mol/(L・min)
C.v (B)=3v (D)
D.v (A)=0.4 mol/(L・min)
5、填空题 工业废水中常含有一定量的Cr2O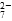 和CrO
和CrO ,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
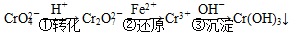
其中第①步存在平衡:
2CrO (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O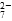 (橙色)+H2O
(橙色)+H2O
(1)若平衡体系的 pH = 2,该溶液显________色。
(2)能说明第①步反应达平衡状态的是________。
a.Cr2O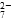 和CrO
和CrO ?的浓度相同
?的浓度相同
b.2v(Cr2O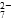 )=v(CrO
)=v(CrO )
)
c.溶液的颜色不变
(3)第②步中,还原 1 mol Cr2O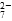 ?离子,需要______mol的FeSO4・7H2O。
?离子,需要______mol的FeSO4・7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)  Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)・c3(OH-)=10-32,要使 c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
方法2:电解法
该法用 Fe 做电极电解含Cr2O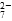 的酸性废水,随着电解的进行,在阴极附近溶液 pH 升高,产生 Cr(OH)3沉淀。
的酸性废水,随着电解的进行,在阴极附近溶液 pH 升高,产生 Cr(OH)3沉淀。
(5)用Fe做电极的原因为______________________________________
(6)在阴极附近溶液 pH 升高的原因是(用电极反应解释)________________,溶液中同时生成的沉淀还有________。