微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 平衡:如化学平衡、溶解平衡、电离平衡。下列不存在平衡的是(不考虑水的电离平衡)
A.稀醋酸水溶液中
B.氢氧化钙悬浊液中
C.二氧化硫与氧气反应的混合物中
D.稀氯化钠水溶液中
参考答案:D
本题解析:A 存在,醋酸是弱酸,存在电离平衡
B 氢氧化钙悬浊液存在沉淀溶解平衡
C 二氧化硫与氧气反应生成三氧化硫,是一个可逆反应
D 稀氯化钠水溶液中,氯化钠是盐,强电解质,不存在平衡问题
故选D
本题难度:简单
2、填空题 (14分)T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示,3分钟时达到平衡;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。?
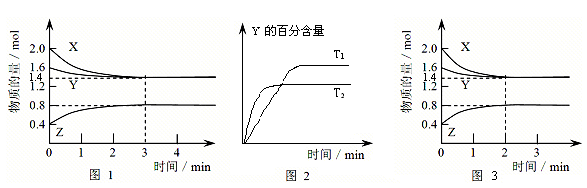
(1)容器中发生的反应可表示为______?________?________?__
(2)该反应的△H?????0(填“>”、“<”或“=”)
判断理由是:______?________?________?________?____?________?__。
(3)反应进行的前3 min内,用X表示的反应速率 v(X)=____________
(4)保持其他条件不变,升高温度,该反应的化学平衡常数K将____________(填“变大”、“减小”或“不变”)
(5)①若改变反应条件,使反应进程如图3所示,则改变的条件是____________
②一定条件下的密闭容器中,该反应达到平衡,要提高气体Y的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压???? b.加入催化剂??? c.增加X的浓度??? d.增加气体Y的浓度???
参考答案:(1)3X(g)+??? Y (g)  本题解析:(1)根据特异性1可知,XY的物质的量分别减少了2.0mol-1.4mol=0.6mol、1.6mol-1.4mol=0.2mol。Z的物质的量增加了0.8mol-0.4mol=0.4mol。所以根据变化量之比是相应的化学计量数之比可知,方程式为3X(g)+Y (g)
本题解析:(1)根据特异性1可知,XY的物质的量分别减少了2.0mol-1.4mol=0.6mol、1.6mol-1.4mol=0.2mol。Z的物质的量增加了0.8mol-0.4mol=0.4mol。所以根据变化量之比是相应的化学计量数之比可知,方程式为3X(g)+Y (g)  2Z(g)。
2Z(g)。
(2)根据图像2可知,T1小于T2,温度高,Y的含量低,说明升高温度平衡向正反应方向移动,所以正反应是吸热反应,即△H大于0.
(3)反应进行的前3 min内,用X表示的反应速率 v(X)= =0.1 mol/(L? min)。
=0.1 mol/(L? min)。
(4)保持其他条件不变,升高温度,平衡平衡向正反应方向移动,平衡常数增大。
(5)①根据图像3可知,平衡状态没有改变,说明改变的条件是加入了催化剂。
②因为正反应是体积减小的、吸热的可逆反应,所以升高温度或增大压强,平衡都向正反应方向移动,转化率增大,a正确。催化剂不能改变平衡状态,b不正确。增加X的浓度,平衡向正反应方向移动,Y的转化量增大,c正确。增加Y的浓度,平衡向正反应方向移动,但Y的转化率降低d不正确,答案选ac。
本题难度:一般
3、计算题 一定温度下,向密闭容器中加入等物质的量的SO2和O2,反应达平衡时,SO2的转化率是50%,此时SO3所占的体积分数为多少?
参考答案:28.57%
本题解析:设反应开始时SO2和O2均为1 mol,则有:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
开始状态:1 mol?????1 mol?????? 0
改变的量:0.5 mol??? 0.25 mol??? 0.5 mol
平衡状态:0.5 mol??? 0.75 mol??? 0.5 mol
SO3的体积分数为:
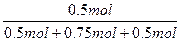 ×100%=28.57%
×100%=28.57%
答:SO3所占的体积分数为28.57%
本题难度:简单
4、计算题 “温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组
| 温度/℃
| 起始量/mol
| 平衡量/mol
| 达到平衡所需时间/min
|
CO
| H2O
| H2
| CO
|
1
| 650
| 4
| 2
| 1.6
| 2.4
| 6
|
2
| 900
| 2
| 1
| 0.4
| 1.6
| 3
|
3
| 900
| a
| b
| c
| d
| t
?
① 实验1条件下平衡常数K=?????(保留小数点后二位数字)。
② 实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值????(填具体值或取值范围)。
③ 实验4,若900℃时,在此容器中加入10molCO、5molH2O、2molCO2、5molH2,则此时v(正)?????v(逆)(填“<”、“>”、“=”)。
(2)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10―9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10―4mo1/L,则生成沉淀所需CaCl2溶液的最小浓度为???。
(3)已知BaSO4(s) + 4C(s) ="4CO(g)" + BaS(s)??△H1 =+571.2kJ/mol,
BaSO4(s) + 2C(s) = 2CO2(g) + BaS(s)??△H2="+226.2" kJ/mol。
则反应C(s) + CO2(g) = 2CO(g)的△H3=??????kJ/mol。
 (4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li ???????LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为:????????????????和?????????????????。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为???????。(Li的相对原子质量约为7.0) (4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li ???????LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为:????????????????和?????????????????。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为???????。(Li的相对原子质量约为7.0)
参考答案:(16分)
(1)①2.67(2分)??②<1
本题解析:
试题分析:(1)①表中实验1有关组分的起始物质的量、平衡物质的量已知,容器体积为2L,由于c=n/V,则
CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g)
起始浓度(mol/L)?????? 2????? 1?????????? 0???? 0
变化浓度(mol/L)?????? 0.8???? 0.8??????? 0.8??? 0.8
平衡浓度(mol/L)?????? 1.2???? 0.2??????? 0.8??? 0.8
K=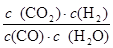 = = =2.67 =2.67
②实验3中CO、H2O的起始浓度分别为a/2mol/L、b/2mol/L,设CO的变化浓度为xmol/L,由于CO、H2O的变化浓度之比等于化学方程式的系数之比,则H2O的变化浓度为xmol/L,则CO、H2O的平衡转化率分别为2x/a、2x/b,若CO的平衡转化率大于水蒸气,则2x/a>2x/b,所以a/b<1;
③先根据实验2中有关数据求900时的平衡常数,再根据温度不变平衡常数不变,利用此时各组分的物质的量计算各自浓度,根据浓度商与平衡常数的大小判断此时反应进行的方向(若浓度商大于平衡常数,则反应向逆反应方向进行,反之,则向正反应方向进行),最后反应向哪个方向进行,则哪个方向的速率就大于相反方向的速率。
表中实验2有关组分的起始物质的量、平衡物质的量已知,容器体积为2L,由于c=n/V,则
CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g)
起始浓度(mol/L)?????? 1???? 0.5????????? 0????? 0
变化浓度(mol/L)????? 0.2??? 0.2????????? 0.2??? 0.2
平衡浓度(mol/L)????? 0.8??? 0.3????????? 0.2??? 0.2
K=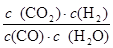 = = =0.167 =0.167
实验4时CO、H2O、CO2、H2的浓度分别为5mol/L、2.5mol/L、1mol/L、2.5mol/L,则Q=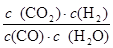 = = =0.2>K=0.167,说明此时反应应该向逆反应方向进行,所以v(逆)>v(正),即v(正)<v(逆); =0.2>K=0.167,说明此时反应应该向逆反应方向进行,所以v(逆)>v(正),即v(正)<v(逆);
(2)设混合前CaCl2溶液的最小浓度为xmol/L,Na2CO3溶液的浓度为2×10―4mo1/L,则等体积混合后CaCl2、Na2CO3的浓度分别为x/2mol/L、1×10―4mo1/L,则Ksp=2.8×10―9= x/2×1×10―4,x=5.6×10―5;
(3)先将3个热化学方程式依次编号为①②③,接着观察它们的关系,发现①/2―②/2=③,则C(s) + CO2(g) = 2CO(g)的△H3=△H1 /2―△H2/2="+172.5" kJ/mol;
(4)放电时电池总反应式为FePO4+Li=LiFePO4,其中锂元素由0升为+1价,铁元素由+3降为+2价,前者在负极上发生氧化反应,后者在正极上发生还原反应,根据电子、电荷、原子守恒原理及电解质中定向移动的离子环境,正极反应式为FePO4+Li++e―=LiFePO4,负极反应式为Li-e―=Li+;用惰性电极电解水的原理为2H2O 2H2↑+O2↑~4e―,则n(H2)=2n(O2),由于n=V/Vm,则n(H2)+n(O2)="3" n(O2)=3.36L÷22.4L/mol=0.15mol,则n(O2)=0.05mol,则转移电子的物质的量="4" n(O2)=0.2mol,由于新型电池中转移电子和电解水时转移电子相等,FePO4+Li=LiFePO4~e―中参加反应的锂与转移电子的系数之比等于物质的量之比,则参加反应的锂为为0.2mol,由于锂的相对原子质量约为7.0,m=n×M,则参加反应的锂为1.4g。 2H2↑+O2↑~4e―,则n(H2)=2n(O2),由于n=V/Vm,则n(H2)+n(O2)="3" n(O2)=3.36L÷22.4L/mol=0.15mol,则n(O2)=0.05mol,则转移电子的物质的量="4" n(O2)=0.2mol,由于新型电池中转移电子和电解水时转移电子相等,FePO4+Li=LiFePO4~e―中参加反应的锂与转移电子的系数之比等于物质的量之比,则参加反应的锂为为0.2mol,由于锂的相对原子质量约为7.0,m=n×M,则参加反应的锂为1.4g。
本题难度:一般
5、选择题 已知常温常压和催化剂条件下,N2(g)和H2(g)生成2 mol NH3(g)放出92.4 kJ的热量。在上述条件下向密闭容器中通入1 mol N2和3 mol H2,达到平衡时放出热量为Q1 kJ;向另一体积相同的容器中通入0.9 mol N2、2.7 mol H2和0.2 mol NH3,相同条件下达到平衡时放出热量为Q2 kJ。则下列关系式正确的是(??? )
A.2Q=Q1="92.4"
B.Q2<Q1<92.4
C.Q1<Q2<92.4
D.Q1=Q2=92.4
参考答案:B
本题解析:根据题意,每生成2 mol NH3放出92.4 kJ热量,1 mol N2和3 mol H2反应,达到平衡态,生成NH3小于2 mol,故放出热量小于92.4 kJ;另一容器中通入0.9 mol N2、2.7 mol H2和0.2 mol NH3,相同条件下达到平衡时与上述平衡是等效平衡,但由于充入了NH3,所以N2和H2反应生成的NH3比上述平衡少,故有Q2<Q1<92.4。
本题难度:简单
|