��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵���������
��NaHCO3��Һ��ˮϡ�ͣ�c��Na������c��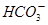 ����ֵ��������
����ֵ��������
��Ũ�Ⱦ�Ϊ0��1mol��L��1��Na2CO3��NaHCO3�����Һ��2c��Na������3[c�� ����c��
����c��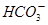 ��]
��]
����0��1mol��L��1��ˮ�еμ�0��1mol��L��1���ᣬǡ����ȫ��Ӧʱ��Һ��pH��a������ˮ���������c��OH������10��a mol��L��1
����0��1mol��L��1��NH4��2SO3��Һ�м�������NaOH���壬c��Na������c��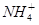 ����c��
����c��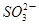 ��������
��������
����Na2Sϡ��Һ�У�c��H������c��OH������2c��H2S����c��HS����
A���٢�
B���ڢ�
C���٢�
D���ڢ�
�ο��𰸣�B
���������
����������ټ�ˮϡ�ͣ�̼�������ˮ��̶��������Ա�ֵ������ȷ������ͬҵ����ѭ�����غ㣬��ԭ�ӣ�̼ԭ��=3:2��������2c��Na������3[c��CO32-����c��HCO3-��+c(H2CO3)]������ǡ����ȫ��Ӧʱ����Һ�е������Ӻ����������Ӷ���ˮ����ģ�������Һ��pH=a������Һ�е�������Ũ��=10-amol/L��������������Ũ��ҲΪ10-amol/L����ȷ���ܼ����������ƹ��壬�ٽ�笠�����ˮ�⣬���������������ˮ�⣬����笠�����Ũ�ȼ�С�������������Ũ�������ݸ�����Һ�������غ㣬��ˮ����������Ӻ�����������Ũ����Զ��ȣ�����д��c��H������c��OH������2c��H2S����c��HS��������ȷ������ѡB��
���㣺��Һ������Ժ���Һ�е�����Ũ�ȱȽ�
�����Ѷȣ�����
2��ѡ���� ��������Һ��ˮϡ�ͣ���Һ��ÿ�����ӵ�Ũ�ȶ��������ӵ���
A.CH3COOH��Һ
B.NaCl��Һ
C.NaOH��Һ
D.FeCl3��Һ
�ο��𰸣�B
���������ϡ��������Һ��ÿ�����ӵ�Ũ�ȶ���������˵������ˮ��(��������)Ҳ������ͼ��ǿ��ǿ���Σ�
�����Ѷȣ�����
3������� ��֪�ס��ҡ����ֱ������ѧ��ѧ�еij������ʣ��������ĿҪ��ش��������⣺
�����Ļ�ѧʽΪRCl3������Һ�ڼ������ɲ�����ʱ�ɷ�����Ӧ��
a.��+H2O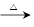 ��+�� b.��
��+�� b.��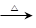 ������+H2O
������+H2O
������Ϊij��;�㷺�Ľ���Ԫ�ص��Ȼ������Һ�������仯�����ɵ�������Ϊ����ɫ��ĩ�������a��Ӧ�Ļ�ѧ����ʽΪ��
������Ϊij�����ڽ���Ԫ�ص��Ȼ����ý��������ڱ��е�λ���ǣ� ��
����30 mL 1 mol/L�ļ���Һ������Ũ��Ϊ4 mol/L��NaOH��Һ��������0.78 g��ɫ������������NaOH��Һ���������Ϊ ��ѡ���ţ�.
A��3 mL
B��7.5 mL
C��15 mL
D��27.5 mL
�۽��������ֽ��������õ������ӣ�����һ��ʢ��NaOH��Һ���ձ��й���ԭ��أ��������ĵ缫��ӦΪ ��
�����ף��ҡ������Ƕ�������ͬһ����Ԫ���γɵĵ��ʻ����������Ϊ���嵥�ʣ��ͱ���Ϊ��̬������ҿɷ�����Ӧ����+�� ������
������
��д��������Ӧ�Ļ�ѧ����ʽ ��
��0.5 mol������������Ĺ������Ʒ�Ӧ��ת�Ƶ��ӵ���ĿΪ
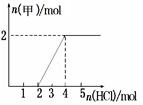
�۽�һ���������ͨ��ijŨ�ȵ�NaOH��Һ����ҺA����A��Һ����ε���ϡ���ᣬ����n(HCl)������n(��)�Ĺ�ϵ��ͼ��ʾ����ҺA�и�����Ũ���ɴ�С��˳��Ϊ ��
�ο��𰸣���FeCl3+3H2O ���������
���������
����������ټ�Ϊ���۽����Ȼ��������ֻ��������������Ϊ���ɵ��Ȼ���Ϊ����ɫ��ĩ�����Լ�һ��ΪFeCl3�������a��Ӧ�Ļ�ѧ����ʽΪ��FeCl3+3H2O Fe(OH)3��+3HCl��
Fe(OH)3��+3HCl��
������Ϊij�����ڽ���Ԫ�ص��Ȼ����ý���ΪAl����Ԫ�����ڱ���λ�ڣ��������ڣ��ڢ�A�壻30 mL 1 mol/L�ļ���Һ��AlCl30.03mol������Ũ��Ϊ4 mol/L��NaOH��Һ������0.78 g��ɫ������Ϊ0.01mol��Al(OH)3������ΪAlCl3��NaOHֱ�ӷ�Ӧ����0.01molAl(OH)3��Al3++3OH?=Al(OH)3�������NaOH��Һ�����Ϊ��0.01mol��3��4mol?L?1=0.0075L=7.5mL��Ҳ����ΪAlCl3��NaOHȫ����Ӧת��ΪAl(OH)3�������μ�NaOH��Һ���ܽⲿ��Al(OH)3��ʣ���Al(OH)3Ϊ0.01mol��Al3++3OH?=Al(OH)3����ҪNaOHΪ3n(Al3+)=0.03mol��3=0.09mol��Al(OH)3+OH? ==AlO2-+2H2O����ҪNaOHΪ0.03mol-0.01mol=0.02mol������ҪNaOH��Һ����0.09mol+0.02mol����4mol?L?1=0.0275L=27.5mL,��BD�
�������ڼ�����Һ�У�ֻ������ʧ���ӷ�����Ӧ������AlΪ������ʧȥ����ת��ΪAlO2-�����Ը�����ӦʽΪ��Al-3e-+4OH-=AlO2-+2H2O��
�ټס��ҡ���Ϊ������Ԫ�أ���Ϊ���嵥�ʣ��ױ�Ϊ���壬�ס��Ҹ��������ɱ��������߾�λ��ͬһ���ڣ�ֻ����ΪC��N��O��Ԫ����ɵĻ�����ۺϷ�����֪����ΪCO2����Ϊ̼����ΪCO�����Ը÷�Ӧ�Ļ�ѧ����ʽΪ��CO2+C 2CO��
2CO��
��������������Ĺ������Ʒ�ӦΪ��2CO2+2Na2O2=2Na2CO3+O2�����ݻ��ϼ۵ı仯�ɵã�CO2 ~ e?������0.5 mol������������Ĺ������Ʒ�Ӧ��ת�Ƶ��ӵ���ĿΪ0.5NA��3.01��1023��
�۸���n(HCl)������n(��)�Ĺ�ϵͼ��������Ҫ��HCl��ȣ�˵����ҺA������ΪNa2CO3���ʸ�����Ũ���ɴ�С��˳��Ϊ��c (Na+) > c(CO32-) > c(OH-) >c(HCO3-)>c(H+)
���㣺���⿼��Ԫ�ػ�������ƶϡ�����ʽ����д�����ݻ�ѧ����ʽ�ļ��㡢ԭ���ԭ��������ת�ơ�����Ũ�ȱȽϡ�
�����Ѷȣ�����
4��ѡ���� ��������ĵ���ƽ�ⳣ�����±���
����
| HCOOH
| HCN
| H2CO3
|
����ƽ�ⳣ��(25��)
| Ki��1.77��10��4
| Ki��4.9��10��10
| Ki1��4.3��10��7
Ki2��5.6��10��11
����ѡ�������ǣ� ��
��2CN����H2O��CO2=2HCN��CO32-
��2HCOOH��CO32-=2HCOO����H2O��CO2��
���к͵��������pH��HCOOH��HCN������NaOH����ǰ��С�ں���
�ܵ��������Ũ�ȵ�HCOONa��NaCN��Һ��������������ǰ��С�ں���
A.�٢� B.�ڢ� C.�ۢ� D.�٢�
�ο��𰸣�D
������������ݵ��볣����֪����HCOOH��H2CO3��HCN��HCO3-��A����B��ȷ�����������pH��HCOOH��HCN��Һ��������HCN��Һ���࣬���к�ʱ���ĵ�NaOH�����࣬C��ȷ�����ݵ���غ㣬n(HCOO��)��n(OH��)��n(Na��)��n(H��)��n(CN��)��n(OH��)��n(Na��)��n(H��)��������������n(Na��)��n(H��)��2������NaCN��ˮ��̶ȴ�NaCN��Һ�е�n(OH��)��n(H��)С��D����
�����Ѷȣ�һ��
5��ѡ���� ��һ�������·������з�Ӧ��������������ˮ�ⷴӦ���ǣ� ? �� A��NH4++2H2O?NH3?H2O+H3O+
B��HCO3-+H2O?H3O++CO32-
C��HS-+H+�TH2S
D��Cl2+H2O?H++Cl-+HClO
�ο��𰸣�A
���������
�����Ѷȣ���
|