微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分) 为了进行氨的催化氧化实验:4NH3+5O2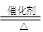 4NO+6H2O。请从下图中选用所需的仪器(可重复使用)组成一套进行该反应的简单装置。现提供试剂:过氧化钠、碱石灰、铂粉、氯化钙、浓硫酸、浓氨水和氢氧化钠溶液。
4NO+6H2O。请从下图中选用所需的仪器(可重复使用)组成一套进行该反应的简单装置。现提供试剂:过氧化钠、碱石灰、铂粉、氯化钙、浓硫酸、浓氨水和氢氧化钠溶液。
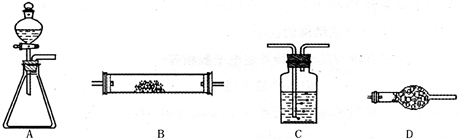
将所选的仪器按连接顺序由上至下依次填入下表(可不填满,也可以补充),并写出该仪器中应加试剂的名称及其作用。
选用的仪器(填字母)
| 加入的试剂
| 作用
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
参考答案:(每个装置3分)
选用的仪器(填字母)
加入的试
本题解析:
试题分析:根据氨的催化氧化原理:4NH3+5O2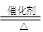 4NO+6H2O。原料必须要提供氧气和氨气,原料中能提供氧气和氨气的应该是浓氨水和过氧化钠反应,仪器是装置A;出来后的气体因为有水蒸气,必须用干燥剂除去,但是因为有氨气,不能选用浓硫酸,只能用碱石灰,选择装置D;在B中进行氨的催化氧化,用到催化剂铂粉;产生的氮氧化物要用氢氧化钠溶液吸收,选择装置C,如果用碱石灰,则选择装置D。 4NO+6H2O。原料必须要提供氧气和氨气,原料中能提供氧气和氨气的应该是浓氨水和过氧化钠反应,仪器是装置A;出来后的气体因为有水蒸气,必须用干燥剂除去,但是因为有氨气,不能选用浓硫酸,只能用碱石灰,选择装置D;在B中进行氨的催化氧化,用到催化剂铂粉;产生的氮氧化物要用氢氧化钠溶液吸收,选择装置C,如果用碱石灰,则选择装置D。
点评:实验设计由于试题较开放,学生答题的思路不好把握,虽然本题难度不大,但是丢分也很容易。
本题难度:一般
2、实验题 (12分)全世界每年被腐蚀损耗的钢铁约占全年钢铁产量的1/10,而在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因。
(1)在潮湿空气中,钢铁发生吸氧腐蚀转化为Fe(OH)2的电池反应方程式为??? ▲???。
(2)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是??? ▲???。(填字母) CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是??? ▲???。(填字母)
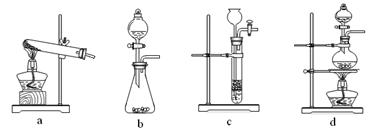
(3)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3・nH2O和Fe两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
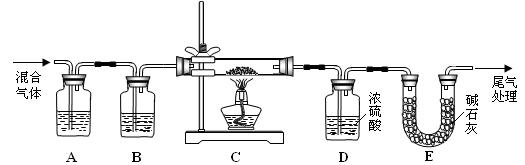
①为得到干燥、纯净的CO气,洗气瓶A、B中盛放的试剂分别是??? ▲???、??? ▲???。
②在点燃酒精灯之前应 进行的操作是:(a)检查装置气密性;(b)?? ▲???。 进行的操作是:(a)检查装置气密性;(b)?? ▲???。
③准确称量样品的质量10.00 g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n =??? ▲??。
④在本实验中,下列情况会使测定结果n偏大的是??? ▲???。(填字母)
a.缺少洗气瓶B?? b.缺少装置E?? c.反应后固体是铁和少量Fe2O3・nH2O
参考答案:共12分。
(1)2Fe + O2 本题解析:略 本题解析:略
本题难度:简单
3、填空题 (11分)物质的分类方法有多种。如根据同一种物质可能属于不同类别进行分类,也可用归纳、比较等方法对物质进行分类等,完成下列题目。
(1)现有①氧气、②空气、③碱式碳酸铜、④氯酸钾、⑤硫、⑥水、⑦氧化镁、⑧氯化钠、⑨氯水、⑩纯醋酸(CH3COOH)、?硫酸钡、?乙醇、?铜等物质。
其中属于单质的有________,属于化合物的有________,其中________属于含氧化合物,________属于氧化物,属于混合物的有________,属于电解质的是________,属于非电解质的有________(均填序号)。
(2)今有下列两组物质,每组中都有一种物质跟其他三种属于不同的种类。将此种物质和分类依据(选出的物质与其他物质不同之处)写在下面相应的表格内。两组物质分别为:
①O2、Cl2、S、N2
②Fe、Na、Al、Si
组别
| 被选出的物质
| 分类依据
| 第①组
| ?
| ?
| 第②组
| ?
| ?
?
参考答案:
(1)①⑤? ③④⑥⑦⑧⑩?? ③④⑥⑦⑩?? ⑥⑦
本题解析:(1)考查同学们对元素化合物知识分类的系统掌握和应用。特别注意两点:①氧化物与含氧化合物的区别;②电解质与非电解质都属于化合物范畴。
(2)考查同学们对于一些常见单质的物理性质和化学性质等方面的异同点的掌握情况,从而对不同物质进行分类。
本题难度:一般
4、实验题 (19分)黄铜矿的主要成分是CuFeS2(硫元素显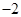 价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下: 价,铁元素显+2价)。实验室里用黄铜矿为原料制取单质铜和铁红(Fe2O3)的流程如下:
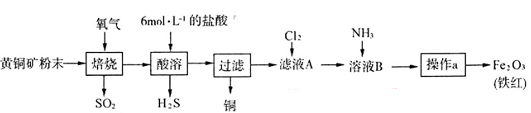
已知:
 ??? ??? = =
(1)在实验室中,应将黄铜矿粉末放在__________(填仪器名称)中焙烧。
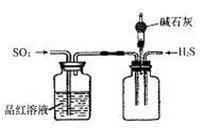
(2)将反应过程中产生的SO2和H2S通入下图所示装置中检验它们的性质。该实验证明SO2具有_________性和__________性。
(3)欲选用下列部分装置在实验室中以MnO2和浓盐酸为原料制取纯净、干燥的氯气。
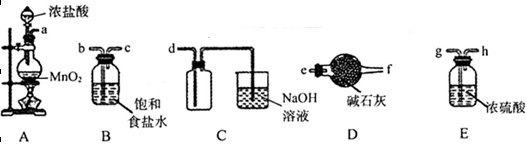
①圆底烧瓶中发生反应的离子方程式为_________________________________________。
②按气流方向由左到右,导管口连接顺序为a→__________________________________。
③装置连接好后,在装药品前,需检验装置的气密性,具体方法是__________________。
④向滤液A中通入C12,某同学取通入C12后的溶液滴加KSCN溶液,用来证明C12的氧化性比Fe3+强的结论。该实验设计是否合理________(填“是”或“否”),请用简要文字解释你的理由_____________________________________________________________。
(4)若使用20 g黄铜矿粉末可制得8 gFe2O3(铁红),则该黄铜矿中含CuFeS2的质量分数是________ (假设各步反应均完全进行且过程中无额外物质损耗)。
参考答案:(19分)
(1)坩埚(2分)
(2)漂白(2分
本题解析:
试题分析:(1)固体的焙烧在坩埚内进行。
(2)SO2通入品红溶液,证明SO2具有漂白性;SO2通入H2S溶液,生成S淡黄色沉淀,证明SO2具有氧化性。
(3)①MnO2与浓盐酸反应生成Cl2、MnCl2、H2O。离子方程式为:MnO2+4H++2Cl? Mn2++Cl2↑2H2O Mn2++Cl2↑2H2O
②生成的Cl2含有HCl、H2O,所以a连接b、c,通过饱和食盐水除去HCl、继续连接g、h,通过浓硫酸,除去H2O,再连接d,即可收集纯净、干燥的氯气。
③利用加热气体膨胀的原理进行装置气密性的检验,所以检验方法为:关闭分液漏斗的活塞,将导管插入水中,微热圆底烧瓶,若导管末端产生气泡,停止加热,导管中有一段水柱形成,说明装置不漏气。
④因为该检验方法是先通入氯气,再滴加KSCN溶液,在通氯气前滤液A中就可能含有Fe3+,无法确定Fe3+一定是Fe2+被Cl2氧化得来的,所以该实验设计不合理。
(4)根据Fe元素守恒可得:2CuFeS2~ Fe2O3,所以该黄铜矿中含CuFeS2的质量分数=8g×368/160÷20g×100%=92%
本题难度:一般
5、实验题 从环己烷可制备1,4-环己二醇的二醋酸酯,下列有关的8步反应(其中所有无机产物都已略去):
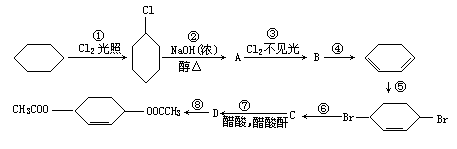
其中有3步属于取代反应,2步属于消去反应,3步属于加成反应。
反应①____和____属于取代反应。
化合物的结构简式是:B____,C_____。
反应④所用试剂和条件是_______。
参考答案:
 本题解析:环己烷在光照条件下发生卤代反应(取代),生成的卤代烃在NaOH醇溶液作用下发生消去反应生成环己烯(A),在不见光的条件与Cl2发生加成反应(请注意与①反应的区别)生成1,2-二氧环己烷(B),再次在NaOH醇溶液作用下发生消去反应生成1,3-环己二烯,第⑤步反应是与Br2发生加成反应(这个反应类似Br2与1,3-丁二烯发生1,4-加成)。由于反应⑦中加入醋酸与醋酸酐发生酯化反应,所以C应该是醇, 本题解析:环己烷在光照条件下发生卤代反应(取代),生成的卤代烃在NaOH醇溶液作用下发生消去反应生成环己烯(A),在不见光的条件与Cl2发生加成反应(请注意与①反应的区别)生成1,2-二氧环己烷(B),再次在NaOH醇溶液作用下发生消去反应生成1,3-环己二烯,第⑤步反应是与Br2发生加成反应(这个反应类似Br2与1,3-丁二烯发生1,4-加成)。由于反应⑦中加入醋酸与醋酸酐发生酯化反应,所以C应该是醇,

2H2O,⑧有机物与 H2发生加成反应。
本题难度:一般
|
|