微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
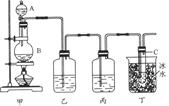
1、实验题 某课外活动小组用如图所示装置制取次氯酸钠。图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸。
完成下列问题:
(1)烧瓶B中盛____________,大试管C中盛____________。
(2)C中发生反应的化学方程式________________________________________________?。
(3)有同学认为可以省去某些装置,你认为怎样?
①能否省去乙装置_________(答“能”或“不能”),理由是_____________________________。
参考答案:②能否省去丙装置__________(答“能”或“不能”),
本题解析:根据氯气的实验装置知,分液漏斗A中盛放的为浓盐酸,烧瓶B中的固体为MnO2,乙装置中盛放饱和NaCl溶液用于吸收挥发出来的盐酸,丙装置中盛放浓硫酸用于干燥氯气,丁装置为尾气吸收装置。
本题难度:简单
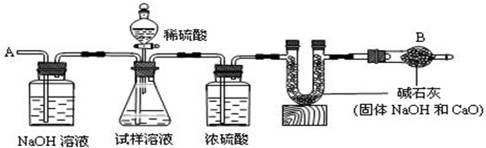
2、实验题 (10分).已知某纯碱试样中含有杂质氯化钠,为测定试样中纯碱的质量分数,可用下图装置进行实验。
主要步骤如下,请填空:
①按图组装仪器,并检查装置的气密性②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;③称量盛有碱石灰的U形管的质量为b g;④从分液漏斗中滴入6mol/L的稀硫酸,直到不再产生气体为止,⑤从导管A处缓缓鼓入一定量的空气;⑥再次称量盛有碱石灰的U形管的质量为c g;⑦重复⑤和⑥的操作,直到U形管的质量基本不变,测得质量为d g。
回答下列问题:(碱石灰是一种干燥剂,不能干燥酸性气体)
(1)装置中干燥管B的作用是???????????????????
(2)如果将分液漏斗中的硫酸换成同浓度的盐酸,测试的结果将???????(填偏高.偏低或不变)
(3)步骤⑤的目的是???????????????
(4)步骤⑦的目的是???????????????
(5)该试样中纯碱的质量分数的计算式为????????????
参考答案:(10分,每空2分)
(1)防止空气中的二氧化碳和水蒸
本题解析:略
本题难度:一般
3、实验题 (15分)已知NaHCO3低温时溶解度小。德榜制碱的方法是:向氨化的饱和食盐水中通入过量的二氧化碳,即有晶体析出,经过滤、 91exam.org洗涤、焙烧得纯碱。此过程可以表示为:
①NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl(此反应是放热反应)
②2NaHCO3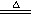 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
现某化学小组根据上述原理在实验室中模拟制碱过程,下图C装置是溶有氨和NaCl的溶液,且二者均达到了饱和。
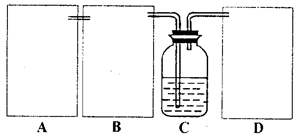
(1)制CO2时为了使反应随开随用,随关随停,上图A方框内应选用以下_________装置(填序号)。简述该装置能随关随停的理由________________。
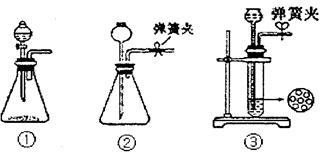
(2)为使实验能够进行,在B、D方框内补上所需装置:_________________(将装置图画在答题卡上),并指明所用试剂:_________________。
(3)该小组同学按正确的方法连接装置,检验气密性合格后进行实验,发现析出的晶体非常少。老师的指导下,他们对某个装置进行了改进,达到了实验目的。你认为他们的改进方法是___________________。
(4)若所用饱和食盐水中含有NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.46g,假设第二步分解时没有损失,则Na2CO3的产率为______________。
参考答案:(1)③(1分),关闭弹簧夹后反应生成的气体使上部压强增大,
本题解析:(1)实验室制取二氧化碳一般采用块状大理石和盐酸反应,要使反应随开随用,随关随停,关键是使固体和溶液分离才能到达目的,故一般采用简易启普发生器,即装置③。原因是关闭弹簧夹后反应生成的气体使上部压强增大,到达一定程度后可把反应液压回漏斗,使固液分离从而停止反应。
(2)因为生成的二氧化碳气体混有氯化氢气体,再通入到C之前要先除杂,试剂选用饱和的碳酸氢钠溶液。由于氨气极易溶于水,所以为了防止倒吸,需要加入1个防倒吸的装置,试剂可以是水或者稀硫酸。
(3)因为NaHCO3低温时溶解度小,所以要大量析出,需要降低溶液的温度。
(4)NaCl的质量为5.85g,所以根据原子守恒可知理论上应得到8.4g碳酸氢钠。由于第二步分解时没有损失,所以Na2CO3的产率是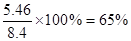 。
。
本题难度:一般
4、选择题 利用下列各组中的物质间反应制备和收集少量相应气体,能采用如下图所示实验装置的是
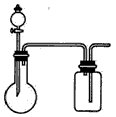 [???? ]
[???? ]
①浓氨水与固体NaOH ②H2O2溶液与二氧化锰 ③稀硝酸与铜片 ④方解石与稀盐酸 ⑤Zn粒与稀盐酸
A.①⑤
B.②④
C.③⑤
D.④⑤
参考答案:A
本题解析:
本题难度:简单
5、实验题 (18分)某兴趣小组欲从工业食盐中精炼精盐,并配制NaCl溶液,请回答下列问题:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A ??????????????????????????B ?????????????????
(2)实验室提纯粗盐的实验操作依次为:
取样、???????、沉淀、过滤、???????、冷却结晶、烘干。
(3)实验室配制500 mL 0.1mol/L的NaCl溶液,具体操作步骤为:①在天平上称取一定质量的NaCl,把它放在烧杯中,用适量的蒸馏水使其完全溶解;②把制得的溶液小心的注入500 mL的容量瓶中;③继续向容量瓶中滴加蒸馏水至液面距刻度线1~2 cm处时,改用胶头滴管小心滴加,直到溶液的凹液面恰好与刻度线相切为止;④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次的洗涤液都转入容量瓶中,并轻轻摇匀;⑤将容量瓶塞好,充分摇匀。试填写下列空白。
①应该称取的NaCl的质量为________,上述操作的正确顺序是____________;
②本实验用到的仪器除玻璃棒、托盘天平、药匙、烧杯外还需要的有___________________、______________________,
③观察容量瓶中的液面时,若俯视刻度线,会使所配的溶液的浓度________(填“偏高”“偏低”或“无影响”,下同)。没有进行操作④,会________;?
参考答案:(1)Ca(OH)2或CaO;? Na2CO3????(2)
本题解析:(1)沉淀剂A来源于石灰窑厂,则A是氢氧化钙或氧化钙。粗盐中含有钙、镁离子等杂质,所以还需要碳酸钠除去钙离子,即B是碳酸钠。
(2)过滤之前需要先溶解,要得到氯化钠晶体,需要蒸发。
(3)①500 mL 0.1mol/L的NaCl中含有0.05mol氯化钠,质量是0.05mol×58.5g/mol=2.925g,所以应该用托盘天平称量2.9g。
②准确配制一定物质的量浓度溶液时需要相应规格的容量瓶,即500ml容量瓶;定容时需要胶头滴管。
③根据c=n/V可知,俯视刻度线,则容量瓶中溶液的体积偏小,浓度偏高;如果没有洗涤,则溶质偏少,浓度偏低。
本题难度:一般