微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (1)下图为常见仪器的部分结构(有的仪器被放大)A图中液面所示溶液的体积为?????mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为N mL,仰视时读数为M mL,若M>N,则所使用的仪器是____????????(填字母标号)。
(2)在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。实验室一般先称取一定质量的KMnO4晶体,粗配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠[Mr(Na2C2O4)=134.0]对粗配的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为:5C2O42-+2MnO4-+16H+→10CO2↑+2Mn2++8H2O

以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.15mol・L-1的高锰酸钾溶液500 mL。
步骤二:准确称取Na2C2O4固体m g放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配高锰酸钾溶液进行滴定。记录相关数据。
步骤三:???????????????????????????????????????????????????????。
步骤四:计算得高锰酸钾的物质的量浓度。试回答下列问题:
①该滴定实验?????????????(“需要”或“不需要”)加指示剂。
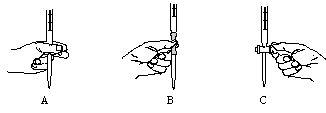
②步骤二中滴定操作图示正确的是__________(填编号)。
③步骤二的滴定过程温度变化并不明显,但操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色明显变快的原因可能是_______?????????????,最后又变慢的原因是?????????。④请写出步骤三的操作内容???????????????????????????。⑤若m的平均数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为?????????????????mol・L-1。
参考答案:(1)28.0;C
(2)①不需要?②A
③
本题解析:(1)四种仪器分别为量筒、容量瓶、滴定管和温度计;A仪器的刻度值为28.0(只能估计出小数点后一位);如果仰视读数大于平视读数,说明刻度是由上至下增大,只有滴定管符合题意
(2)①由于KMnO4溶液本身为紫红色,故不需要指示剂
②KMnO4溶液具有强氧化性,可腐蚀橡胶管,只能盛装在酸式滴定管中,故A操作正确:应用左手握住活塞,拇指与食指转动
③中间阶段褪色明显变快,可能是生成的Mn2+起到催化作用,加快了反应速率;而随着反应的进行,反应物的浓度逐渐减小,导致最后速率又变慢
④中和滴定实验需要进行多次测量,求平均的方法来减少误差,故重复步骤二(两到三次)
⑤由5C2O42-~2MnO4-可知,c(KMnO4)= 0.1600mol・L-1
0.1600mol・L-1
本题难度:一般
2、实验题 (14分)用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s) + H2SO4(98%)==Na2SO4 + H2O + SO2↑

(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。Ⅰ、Ⅱ、Ⅲ处连接的装置分别是__、__、__。

(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作顺序是????????????????????????。
(3)甲处导管的作用是?????????????????????????。
(4)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为???%(用含a、b的代数式填写)
(5)尾端球形干燥管的作用是??????????????????。
参考答案:(1)B A E或B A C(3分)
(2)先加热催化
本题解析:略
本题难度:简单
3、实验题 (8分)某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置。请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题。
供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒。
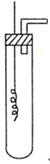
(一)实验步骤:
(1)实验开始时,必须进行的第一步操作是检验装置的???????????;
(2)向试管中加入一定量的固体药品?????????,其目的是?????????????????????????????????????;然后向试管中倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞;
(3)反应一段时间后,用蘸有NaOH溶液的棉花团封住导管口;
(4)将铜丝 向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是????????????????????????????????;
向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是????????????????????????????????;
(5)将注射器插入试管口的橡皮塞中,向试管内推入空气,现象是
??????????????????????????????????????????????????????????????;
(二)问题探究:分别将等质量的铜片与等体积过量的浓、稀硝酸反应,所得溶液前者
呈绿色、后者呈蓝色,某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确?
???????????(填“正确”或“不正确”),理由是????????????????????????????????
????????????????????????????????????????????????????? ??????????????????????
??????????????????????
参考答案:(8分)(一)(1)气密性;(1分 本题解析:略
本题解析:略
本题难度:一般
4、实验题 某课外研究小组,利用下列实验装置来完成“铁与水蒸气的反应”的实验,并检验气体产物。大试管中盛放是:
(1)Mg(OH)2 ,在受热分解后能产生350℃的水蒸气,使得反应获得足够高的热量;
(2)铁粉和铁丝网,铁丝网的作用是为了加大铁粉与水蒸气的接触面,并加大传热的效率。该实验能加快反应的速率,提高实验的成功率。
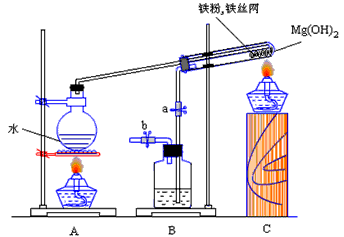
请你回答下列问题:
(1)写出铁与水蒸气反应的化学方程式______________。
(2)装置B中盛放的是___________,其作用是_____________。
(3)在实验进行前必须进行的操作是____________;为了检验导管口b处的气体,在检验前必须进行的操作是__________;
(4)实验完毕后的操作是____________。
参考答案:(1)3Fe+4H2O(g)![]() 本题解析:
本题解析:
本题难度:一般
5、选择题 如图所示:烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻震荡烧瓶,然后打开弹簧夹,烧杯中的液体呈喷泉状喷出,则a、b不可能是???
 ??
??
A.a为HCl,b为H2O
B.a为CO2,b为浓NaOH溶液
C.a为Cl2,b为饱和NaCl溶液
D.a为NH3,b为浓NH4Cl溶液
参考答案:C
本题解析:
试题分析:氯化氢、氨气极易溶于水,可以做喷泉实验。CO2也能被氢氧化钠溶液吸收,瞬间使越强降低,也能形成喷泉。氯气不能溶解在饱和的氯化钠溶液中,不能形成喷泉,答案选C。
点评:该题是中等难度的试题,主要是考查学生对喷泉实验原理以及形成条件的了解掌握程度,有助于培养学生的逻辑推理能力和严谨的实验设计。该题趣味性强,易于调动学生的学习兴趣和学习积极性。
本题难度:简单