微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。
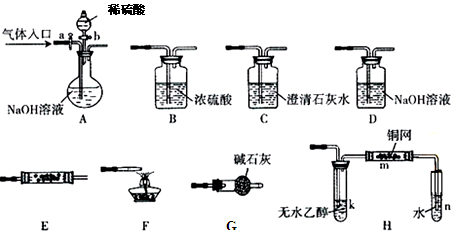
(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为 (填代号)。能验证CO氧化产物的现象是 。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应 ,活塞b应 ,需要加热的仪器装置有 (填代号),m中反应的化学方程式为: 。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有 。
②实验中观察到E内有红棕色气体出现,证明氨气具有 性。
参考答案:(1)ACBECF(2分)?? AB之间的C装置中溶液保持澄
本题解析:
试题分析:(1)用A装置的NaOH来除CO中混有的CO2,(生成Na2CO3),用C装置检验有没有除尽CO2,B装置是干燥气体的,纯净的CO,通入E中,生成的CO2能使装置C有沉淀,多余的CO在装置F处尾气吸收。
(2)关闭装置A的活塞a,停止通入CO和CO2,打开活塞b,使稀硫酸和A中的碳酸钠反应,产生CO2,通入E,和Na2O2,产生O2,用D吸收O2混有的CO2,用B干燥O2中的H2O,纯净的O2在H中和乙醇发生催化氧化反应。加热k产生乙醇蒸汽,加热m ,是因为乙醇催化氧化需要催化剂铜和加热条件。
(3)这过程发生的反应为4NH3+5O2=4NO+6H2O(NH3表现还原性);2NO+O2=2NO2(红棕色)。
本题难度:一般
2、实验题 (12分)某化学学习小组采用下图所提供的仪器装置(夹持仪器已略去)设计实验:验证浓硝酸的氧化性。实验表明浓硝酸能将NO氧化成NO2,由此得出的结论是浓硝酸具有氧化性。
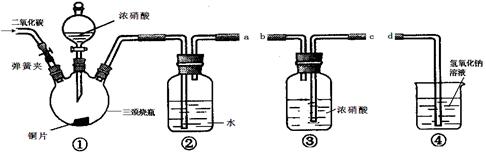
试回答有关问题:
(1)仪器接口的连接顺序为___________????????????????? ____________;
(2)按(1)中连接顺序安装好装置后下一步的操作是___??????????? ____;
加入药品后,打开弹簧夹,通入CO2一段时间,通入CO2的目的是___________________________________________________;
关闭弹簧夹,将装置④中的导管末端伸入氢氧化钠溶液中是为了_________________??????????????? __________________;
(3)装置②发生反应的化学方程式是___________________________________;
(4)该小组得出的结论所依据的实验现象是_____________________________。
参考答案:(1)a→c→b→d??
(2)检验装置气密性;排尽装
本题解析:(1)①是气体的发生装置,浓硝酸和铜反应生成NO2,NO2溶于水即生成NO,所以要检验浓硝酸的氧化性,需要把NO通入到浓硝酸中,氮的氧化物属于大气污染物,需要进行尾气处理,因此最后要通入到氢氧化钠溶液中,即顺序为a→c→b→d。
(2)装置连接好以后,必须最÷检验装置的气密性。因为空气中的氧气也能氧化NO,所以为了防止干扰,需要排尽装置中的空气。
(3)NO2溶于水的方程式为3NO2+H2O=2HNO3+NO。
(4)NO是无色,被氧化生成NO2后气体颜色变为红棕色,所以当②中逸出的无色气体通过③时变成红棕色,即说明结论是正确的。
本题难度:一般
3、选择题 实验室为了制取干燥的氨气,下列方法中适合的是(?)
A.NH4Cl和H2SO4(浓)混合加热,生成的气体用碱石灰干燥
B.N2 + H2→ NH3,用烧碱干燥
C.氯化铵和氢氧化钙固体混合加热,气体用碱石灰干燥
D.向浓氨水中加入生石灰,气体用P2O5干燥
参考答案:C
本题解析:
正确答案:C
A、得不到氨气,生成HCl气体;
B、是工业制氨气;
C、正确;
D、不能用酸性干燥剂。
本题难度:简单
4、实验题 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2・6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5为77.1℃;C2H5OH为78.3℃;C2H5OC2H5(乙醚)为34.5℃;CH3COOH为118℃。实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸,边加热蒸馏。由上面的实验可得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)反应中加入的乙醇是过量的,其目的是????????????????????????????????????。
(2)边滴加醋酸,边加热蒸馏的目的是??????????????????????。
将粗产品再经下列步骤精制:
(3)为除去其中的醋酸,可向产品中加入?????????(填字母)。
A.无水乙醇??????? B.碳酸钠粉末??????? C.无水醋酸钠
(4)再向其中加入饱和氯化钙溶液,振荡,分离,其目的是???????????????????。
(5)然后再向其中加入无水硫酸铜,振荡,其目的是??????????????????。最后,将经过上述处理后的液体加入另一干燥的蒸馏瓶内,再蒸馏,弃去低沸点馏分,收集沸点在76℃~78℃之间的馏分即得纯净的乙酸乙酯。
参考答案:(1)增大反应物乙醇的浓度,有利于反应向生成乙酸乙酯的方向进
本题解析:
试题分析:(1)制取乙酸乙酯的反应是可逆反应,增大反应物乙醇的浓度,有利于反应向生成乙酸乙酯的方向进行;
(2)乙酸乙酯、乙醇、乙醚的沸点较低,边加醋酸边蒸馏,目的使产品蒸出,减小乙酸乙酯的浓度,同时增大醋酸的浓度,使平衡正向进行;
(3)乙酸乙酯不溶于水,醋酸与碳酸钠反应生成醋酸钠、水、二氧化碳气体,所以溶于水的物质在下层,不溶于水的乙酸乙酯在上层,分液可使混合物分离,因此除去产品中的醋酸,应选择碳酸钠溶液,答案选B;
(4)粗产品中仍含有乙醇、乙醚、水,其中乙醇可以和氯化钙反应生成微溶于水的CaCl2・6C2H5OH,所以加入饱和的氯化钙溶液,目的是除去粗产品中的乙醇;
(5)无水硫酸铜与水结合生成蓝色的CuSO4・5H2O,所以加入无水硫酸铜,振荡,其目的是除去粗产品中的水,然后蒸馏可得乙酸乙酯。
本题难度:一般
5、实验题 (8分)病人输液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
 ???
???
(1)该注射液中葡萄糖的物质的量浓度? ___________________。
(2)配制上述l L溶液所需的仪器有:量筒、烧杯、玻璃
棒、托盘天平、药匙、_____________、______________。(在横线上填写所缺仪器的名称)(3)在1L此溶液的配制过程中,下列操作或说法正确 的是_________________。
A.配制过程中加水时不慎超过了刻度线,把水吸出后再加水刚好至刻度线
B.用托盘天平可以准确称量计算所得葡萄糖的质量
C.用胶头滴管加水时,仰视观察凹液面与容量瓶刻度线相切会导致结果偏低
D.容量瓶使用前未干燥,不会影响实验结果
参考答案:
 本题解析:(1)由标签可以知道,500mL葡萄糖注射液中含有的葡萄糖的质量为25g,所以该葡萄糖注射液中葡萄糖的物质的量浓度为
本题解析:(1)由标签可以知道,500mL葡萄糖注射液中含有的葡萄糖的质量为25g,所以该葡萄糖注射液中葡萄糖的物质的量浓度为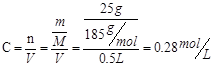
(2)配制500mL一定物质的量浓度的溶液所需的仪器除了量筒、烧杯、玻璃棒、托盘天平、药匙外,还有500mL容量瓶和胶头滴管.
(3)配制过程中若加水超过了刻度线会使浓度偏低只能倒掉重新配制,A错误;用托盘天平可以准确的称量出50g葡萄糖,B正确;胶头滴管定容时若仰视会导致加入的水超过刻度线溶液体积增大,所得到的溶液的浓度会偏小,C正确;容量瓶在操作过程中还会加入蒸馏水所以使用前有水不会对结果产生影响,D正确。
本题难度:一般