微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:
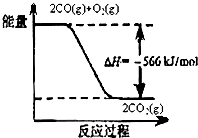
(1)如图
(2)25℃、101kPa下:
①2Na?(s)+
1
2
O2(g)═Na2O(s)△H1=-414kJ/mol
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol
根据以上信息判断,下列说法正确的是( )
A.CO的燃烧热为283?kJ
B.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
C.25℃、101?kPa下,Na2O2(s)+2Na(s)═2Na2O(s)??H=-317?kJ/mol
D.Na2O?和Na2O2阴阳离子个数比不相等
参考答案:C
本题解析:
本题难度:一般
2、简答题 1840年盖斯根据一系列实验事实得出规律,他指出:“若是一个反应可以分步进行,则各步反应的吸收或放出的热量总和与这个反应一次发生时吸收或放出的热量相同.”这是18世纪发现的一条重要规律,称为盖斯定律.已知1mol?金刚石和石墨分别在氧气中完全燃烧时放出的热量为:金刚石,395.41kJ;石墨,393.51kJ.则金刚石转化石墨时,放热还是吸热?______,其数值是_______,由此看来更稳定的是______.若取金刚石和石墨混合晶体共1mol?在O2中完全燃烧,产生热量为QkJ,则金刚石和石墨的物质的量之比为______(用含Q的代数式表示).
参考答案:由盖斯定律可知,要得到金刚石转化为石墨的热量变化,可将二者在
本题解析:
本题难度:一般
3、填空题 按照盖斯定律,结合下列反应方程式,回答问题。已知:
(1)NH3(g)+HCl(g)=NH4Cl(s) △H=-176KJ·mol-1
(2)NH3(g)+H2O(l)=NH3·H2O(aq) △H=-35.1KJ·mol-1
(3)HCl(g)+H2O(l)=HCl(aq) △H=-72.3KJ·mol-1
(4)NH3·H2O(aq)+ HCl(aq)=NH4Cl(aq)+ H2O(l) △H=-52.3KJ·mol-1
(5)NH4Cl(S)+ H2O(l)= NH4Cl(aq) △H=Q
则第(5)个方程式中的反应热是_________________________
参考答案:+16.3kJ·mol-1
本题解析:
本题难度:一般
4、填空题 研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。
已知:①CO(g)+?12O2(g)=CO2(g)???△H=-283.0kJ·mol-1???
②S(s)+?O2(g)=SO2(g)?????△H=-296.0kJ·mol-1?
此反应的热化学方程式是___________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知: ?????
①?CO(g)+NO2(g)=NO(g)+CO2(g)???△H=-akJ·mol-1?(a>0) ?????
②?2CO(g)+2NO(g)=N2(g)+2CO2(g)???△H=-bkJ·mol-1?(b>0)
若用标准状况下?3.36LCO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为_______mol,放出的热量为_______?kJ(用含有a和b的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如: ?????
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)????△H1=-574kJ·mol-1?① ?????
②CH4(g)+4NO?(g)=2N2(g)+CO2(g)+2H2O(g)????△H2=?②
若1molCH4还原NO2至N2整个过程中放出的热量为867kJ,则△H2=___________?。
参考答案:(1)2CO(g)+SO2(g)=S(s)+2CO2(g)
本题解析:
本题难度:一般
5、选择题 已知25℃、101 kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O2(g)=CO2(g) ; △H=-393.51 kJ·mol-1
C (金刚石) +O2(g)=CO2(g) ; △H=-395.41 kJ·mol-1
据此判断,下列说法正确的是 [???? ]
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
参考答案:A
本题解析:
本题难度:一般
|