��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� �������������ͼ��ʾ��ʵ��װ�ã�Ŀ����������ˮ��Ӧ��ʵ�鲢��֤�����Ƶ��������ʣ�������ˮ��Ӧ�IJ�����ʲô��
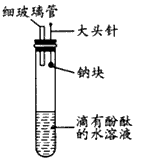
(1)�������ʵ�����ʱ����Ҫ��������____��
(2)��ν��в�����
(3)ʵ��������___��
�ο��𰸣�(1)С�Թܺ;ƾ���
(2)����ͷ�������ᣬʹ�ƿ���
���������
�����Ѷȣ�һ��
2��ѡ���� Ϊ̽��һ�廷����( )��NaOH�Ĵ���Һ���ȷ�������ˮ�ⷴӦ������ȥ��Ӧ���ס��ҡ�����λͬѧ�ֱ������������ʵ�鷽�����ף���Ӧ���Һ�е���ϡ�����к�NaOH��Ȼ���ٵ���AgNO3��Һ������dz��ɫ�����������֤����������ȥ��Ӧ���ң���Ӧ���Һ�е�����ˮ������Һ��ɫ�ܿ���ȥ�����֤����������ȥ��Ӧ��������Ӧ���Һ�е�������KMnO4��Һ������Һ��ɫ��dz�����֤����������ȥ��Ӧ��������ȷ���� [???? ]
)��NaOH�Ĵ���Һ���ȷ�������ˮ�ⷴӦ������ȥ��Ӧ���ס��ҡ�����λͬѧ�ֱ������������ʵ�鷽�����ף���Ӧ���Һ�е���ϡ�����к�NaOH��Ȼ���ٵ���AgNO3��Һ������dz��ɫ�����������֤����������ȥ��Ӧ���ң���Ӧ���Һ�е�����ˮ������Һ��ɫ�ܿ���ȥ�����֤����������ȥ��Ӧ��������Ӧ���Һ�е�������KMnO4��Һ������Һ��ɫ��dz�����֤����������ȥ��Ӧ��������ȷ���� [???? ]
A.��
B.��
C.��
D.����ʵ�鷽��������ȷ
�ο��𰸣�D
���������
�����Ѷȣ���
3��ѡ���� ����9ͼ��ʾ��ʵ���У��ܴﵽʵ��Ŀ�ĵ���
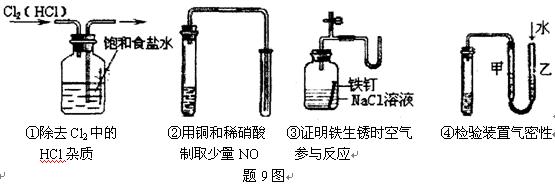
A���٢ڢۢ�
B���ڢۢ�
C���ۢ�
D���٢�
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
4��ʵ���� ��ȤС���ѧ������Mg��CO2��Ӧԭ���Ʋ���Ҳ����CO2��ȼ�գ�Ϊ��ȷ������ﲢ����ʵ����֤��ijͬѧ���������װ�ý���ʵ��(��֪PdCl2�ܱ�CO��ԭ�õ���ɫ��Pd)����ش���������
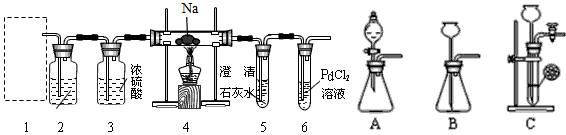
��1����ͼװ��2��Ӧʢ��___________��Һ��д��ѧʽ����
��2��Ϊ��ʹ��Ӧ�濪���ã������ͣ����ͼ������Ӧѡ��__________װ�ã�����ͼ��ĸ���ţ���
��3�����װ�õ���������ò�װ��ҩƷ���ڵ�ȼ�ƾ���ǰ��Ӧ�Ƚ���1װ�õIJ�������װ��_______�������ֱ�ţ��г���__________����ʱ���ٵ�ƾ��ƣ��ⲽ������Ŀ����____________________
��4������װ��6���к�ɫ�������ɣ�װ��4�в������壨ֻ��һ�����ʣ������������ʹ����ʯ��ˮ����ǵ�����ų��������������̼��Ӧ�Ļ�ѧ����ʽΪ______________________________��
����װ��6����Һ����������װ��4�в������壨���������ʣ������������ʹ����ʯ��ˮ����ǵ�����ų��������������̼��Ӧ�Ļ�ѧ����ʽΪ______________________________��
��5��ָ����ʦ��Ϊ������Ҫ��������������Ƿ���̼���ƻ�Ҫ���������Ƿ��������ƺ�̼����ȷ���Ƴ�ַ�Ӧ���������һ����ʵ�飬��֤װ��4�еIJ����������Ƿ���Na2O��C��________________________________________________________________________________
�ο��𰸣���1������NaHCO3?
��2��C
��3��5��
���������
�����Ѷȣ�����
5��ʵ���� ��20�֣�ij�о���ѧϰС����ʵ����������0.20mol��L-1���������Һ��Ȼ������ζ�ijδ֪Ũ�ȵ�����������Һ��
�����ƴ���Һ����1��7 g������������(�������ᷴӦ)�Ĺ����ռ���Ʒ���Ƴ�200 mL��Һ���������Ҫ�����������ձ���200 mL����ƿ����Ͳ������???????????????�p????????????????��
�Ƶζ���
��ʢװ0.20mol��L-1�����ҺӦ����??????????????ʽ�ζ��ܣ�
�ڵζ�ʱ��������ƿ�мӷ�̪��Ϊָʾ��������εζ����۲쵽??????????????ʱΪ�ζ��յ㡣
���й����ݼ�¼���£�
����
| ����Һ�����(mL)
| ���������Һ�����(mL)
|
��ʼ����
�ζ�ǰ
| �յ����
|
1
| 20.00
| 0.50
| 20.40
|
2
| 20.00
| 6��00
| 26��10
|
3
| 20.00
| 4��00
| 24��00
?
���ݴ�����NaOH��Һ��Ũ��Ϊ?????mol��L-1���ռ���Ʒ�Ĵ���Ϊ??????����������λ��Ч���֣�
���Է������¸��������ʵ�����Ŀ���Ӱ�죬�á�ƫ�ߡ��p��ƫ�͡�����Ӱ�족����գ�
����������ˮ��ϴ��ƿ�����ʹ�ⶨ�Ľ��??????????????��
�����ڵζ������в�����������Һ������ƿ�⣬���ʹ�ⶨ���??????????????��
�����ռ���ָʾ���ֲ�����ɫ�б仯��ֹͣ�ζ������ʹ�ⶨ���??????????????��
�ܶ���ʱ�����ζ�ǰ���Ӷ������ζ������Ӷ��������ʹ�ⶨ���??????????????��
�ο��𰸣���1����ͷ�ι� �������� ��??????
��2�� ����
���������
��������������ƴ���Һ����1��7 g������������(�������ᷴӦ)�Ĺ����ռ���Ʒ���Ƴ�200 mL��Һ���������Ҫ�����������ձ���200 mL����ƿ����Ͳ�����н�ͷ�ιܡ����������� �������ҺӦ������ʽ�ζ��ܣ��ڵζ�ʱ��������ƿ�мӷ�̪��Ϊָʾ��������εζ������ڿ�ʼʱ��̪�ڼ�����Һ�У���˵ζ�ǰ��ҺΪ��ɫ�����۲쵽�μ����һ�����ᣬ��Һ�ɺ�ɫ�����ɫ�Ұ���Ӳ��ָ�ʱ�ζ��ﵽ���յ㡣�۵�һ�εμ��������Ϊ19��90ml;�ڶ��εμ��������Ϊ��20.10ml;�����εμ��������Ϊ20.00ml�����ƽ������HCl�����Ϊ��(19��90ml��20.10ml+20.00ml)��3=20.00ml���������ǡ����ȫ�к�ʱ���ߵ����ʵ�����ȿɵ�c(NaOH)="c(HCl)��V(HCl)/v(NaOH)=" (0.20mol/L��20.00ml) ��20.00ml=" 0.20" mol/L��n(NaOH)=0.20mol/L��0.02L��10=0.04mol��m(NaOH)=0.04mol��40g/mol=1��6g������NaOH�Ĵ���Ϊ��(1��6g��1��7g)��100%=94��1�����Ǣ���������ˮ��ϴ��ƿ����������ƿ�м������ʵ������䣬���Բ���ʹ�ⶨ�Ľ����������Ӱ�졣�����ڵζ������в�����������Һ������ƿ�⣬�����ĵı�����Һ�����ƫ���Դ�Ϊ����ʹ�ⶨ���ƫ�ߡ������ռ���ָʾ���ֲ�����ɫ�б仯��ֹͣ�ζ��������ĵı�����Һ�������ƫС���Դ�Ϊ������Ľ����ƫ�͡��ܶ���ʱ�����ζ�ǰ���Ӷ�������ʼ����ƫС���ζ������Ӷ������ζ��յ����ƫ���Դ�Ϊ������Ľ����ƫ�ߡ�
�����Ѷȣ�һ��
|