微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用石墨作电极电解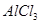 溶液时,图12-5所示的电解变化曲线合理的是
溶液时,图12-5所示的电解变化曲线合理的是
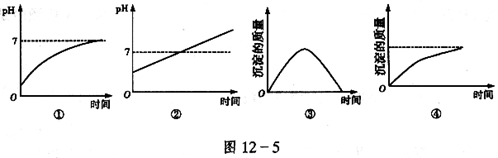
A.①④
B.②④
C.②③
D.①③
参考答案:A
本题解析:电解开始一段时间:
阳极:2Cl-- 2e- = Cl2↑、阴极:2H20 +2e-= H2↑+ 2OH-
总反应:2AlCl3+6H20=2Al(OH)3↓+3H2↑+3Cl2↑
当AlCl3全部电解反应完之后,就等于再电解水:
阳极反应:4OH―-4e―=2H2O+O2↑
阴极反应:2H++2e―=H2↑
总反应:2H2O=(通电)2H2↑+O2↑
所以不会有多余的OH―,溶液PH不会大于7,Al(OH)3沉淀也不会溶解
故答案为A
本题难度:一般
2、选择题 Li-SO2电池具有输出功率高且低温性能好的特点,其电解质为LiBr,溶剂是碳酸丙烯酯和乙腈,Li+可在其中移动。电池总反应式为:2Li +2SO2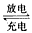 Li2S2O4,下列有关该电池的说法正确的是 [???? ]
Li2S2O4,下列有关该电池的说法正确的是 [???? ]
A.该电池总反应为可逆反应
B.充电时阴极反应式为:Li++e-=Li
C.放电时Li+向负极移动
D.该电池电解质溶液可换成LiBr水溶液
参考答案:B
本题解析:
本题难度:一般
3、选择题 用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质(中括号内),溶液能与原来溶液完全一样的是
A.CuCl2[CuCl2溶液]
B.AgNO3[Ag2O]
C.NaCl [HCl溶液]
D.CuSO4[Cu(OH)2]
参考答案:B
本题解析:
试题分析:电解池中,要想使电解质溶液复原,遵循的原则是:电解后从溶液中减少的物质是什么就利用元素守恒来加什么。A、电解氯化铜时,阳极放氯气,阴极生成金属铜,所以应加氯化铜固体让电解质溶液复原,故A错误;B、电解硝酸银时,阳极产生氧气,阴极产生银,所以应加Ag2O让电解质溶液复原,故B正确;C、电解氯化钠时,阳极产生氯气,阴极产生氢气,所以通入氯化氢气体让电解质溶液复原,故C错误;D、电解硫酸铜时,阳极产生氧气,阴极产生金属铜,所以应加氧化铜让电解质溶液复原,故D错误,答案选B。
本题难度:一般
4、选择题 如图a、b、c、d均为石墨电极,通电进行电解。下列说法不正确的是???????
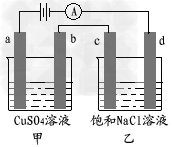 [???? ]
[???? ]
A.甲中a电极反应式为4OH--4e-=O2↑+2H2O
B.当b极有64gCu析出时,c电极产生2g气体
C.电解后向乙中通入适量HCl气体,溶液组成可以恢复
D.电解时向乙中滴入酚酞试剂,d电极附近变红
参考答案:B
本题解析:
本题难度:一般
5、填空题 钛铁矿的主要成分为FeTiO3(可表示为FeO・TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如图所示:
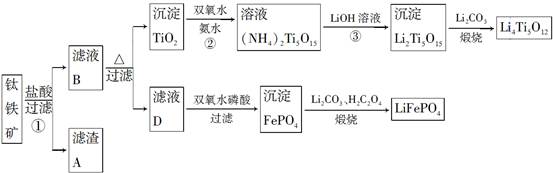
已知:FeTiO3与盐酸反应的离子方程式为FeTiO3+4H++4Cl-=Fe2++TiOCl42―+2H2O
(1)化合物FeTiO3中铁元素的化合价是________。
(2)滤渣A的成分是________。
(3)滤液B中TiOCl42―转化生成TiO2的离子方程式是________________。
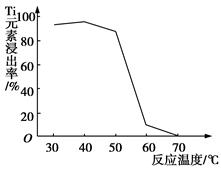
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti元素浸出率下降的原因是________________________________。
(5)反应③的化学方程式是________________________。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是________。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)做电极组成电池,其工作原理为Li4Ti5O12+3LiFePO4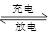 Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
参考答案:(1)+2
(2)SiO2
(3)TiOCl42
本题解析:(2)钛铁矿中只有SiO2不与盐酸反应,因此滤渣A的成分是SiO2。(3)TiOCl42―转化为TiO2,Ti的化合价不变,发生的是TiOCl42―的水解反应。(5)反应③为LiOH与(NH4)2Ti5O15的复分解反应。(6)根据得失电子守恒,可得关系 式:2Fe2+~H2O2~2Fe3+~H2C2O4,则17%双氧水与H2C2O4的质量比=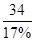 本题难度:困难
本题难度:困难