微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)① 硫在氧气里燃烧 ② 红磷在氧气里燃烧 ③ 铁丝在氧气里燃烧 ④ 铝箔在氧气里燃烧对上述4个化学反应可以从不同的角度分类:____________、_____________、______________。(至少分三类)
(2)阅读、分析下列两个材料:
材料一:
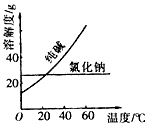
材料二:
|
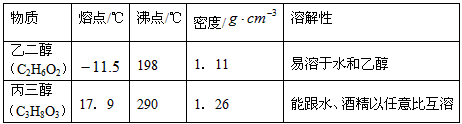
回答下列问题(填序号):
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
① 将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用______________。
② 将乙二醇和丙三醇相互分离的最佳方法是________________。
参考答案:(1)化合反应;氧化还原反应;非离子反应
(2)①C;
本题解析:
本题难度:一般
2、填空题 (17分)过氧化钙(CaO2)难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,用作杀菌剂、防腐剂、解酸剂、油类漂白剂及封闭胶泥的快干剂,在食品、牙粉、化妆品等制造中用作添加剂。下图是以大理石(主要杂质是氧化铁)等为原料制取过氧化钙(CaO2)的流程。
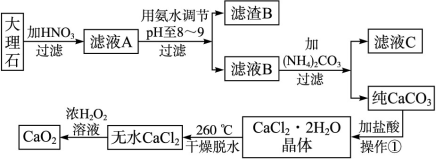
请回答下列问题:
(1)操作①中应包括?????????、?????????、?????用氨水调节pH至8~9的目的是______________。
(2)若测得滤液C中c(CO )=2.50×10-4 mol・L-1,则Ca2+_?_____(填“是”或“否”)沉淀完全。[已知c(Ca2+)≤10-5 mol・L-1可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
)=2.50×10-4 mol・L-1,则Ca2+_?_____(填“是”或“否”)沉淀完全。[已知c(Ca2+)≤10-5 mol・L-1可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(3)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中,c(NH )????????c(NO
)????????c(NO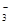 ) (填 > 、< 或 = ),(NH4)2CO3溶液中离子浓度由大到小的顺序为???????????????。
) (填 > 、< 或 = ),(NH4)2CO3溶液中离子浓度由大到小的顺序为???????????????。
(4)在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,写出该反应的化学方程式:_______________,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9~11,才出现大量沉淀。用简要的文字解释需用氢氧化钠调节pH至9~11的原因_________________________。
(5)写出CaO2与H2O反应的化学方程式??????????????????????????????????????。
参考答案:(1)溶解、过滤、蒸发结晶(3分);除去Fe3+或使Fe3+
本题解析:
试题分析:(1)沉淀碳酸钙用盐酸溶解然后蒸发结晶可以得到氯化钙晶体;因大理石中的主要杂质是氧化铁,它与硝酸反应生成了Fe(NO3)3,在调节pH到8~9时,Fe3+会以Fe(OH)3沉淀形式进入滤渣,从而除去了杂质离子Fe3+。
(2)根据离子积Ksp(CaCO3)=4.96×10-9=c(Ca2+)・c(CO ),得c(Ca2+)=4.96×10-9/2.50×10-4 mol・L-1=1.98×10-5 mol・L-1 > 10-5 mol・L-1,没有沉淀完全。
),得c(Ca2+)=4.96×10-9/2.50×10-4 mol・L-1=1.98×10-5 mol・L-1 > 10-5 mol・L-1,没有沉淀完全。
(3)由电荷守恒:c(H+)+c(NH )=c(OH-)+c(NO
)=c(OH-)+c(NO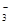 ),因c(H+)>c(OH-),故c(NH
),因c(H+)>c(OH-),故c(NH )<c(NO
)<c(NO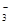 )。
)。
(4)由CaCl2+H2O2 CaO2+2HCl,加入NaOH溶液,NaOH与HCl发生中和反应,减少了生成物浓度,使上述平衡向正反应方向移动,有利于CaO2沉淀的生成。
CaO2+2HCl,加入NaOH溶液,NaOH与HCl发生中和反应,减少了生成物浓度,使上述平衡向正反应方向移动,有利于CaO2沉淀的生成。
(5)CaO2中O元素的化合价为―1价,部分化合价升高转化为O2,部分化合价降低转化为Ca(OH)2,所以化学方程式为:2CaO2+2H2O=2Ca(OH)2+O2↑
本题难度:困难
3、实验题 某化学小组同学为了验证日常生活所用火柴头中的化学成分(含KClO3、MnO2、S等),设计了以下实验流程(见图-1):?

试回答以下问题:
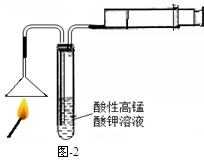
(1)燃着的火柴按图-2进行实验,若试管中能观察到?????????????????的现象,则可证明火柴头中含有硫元素。图中针筒的作用是??????????????。
(2)为了证明火柴头中含有氯元素,后续的实验步骤是??????????????????????????????。
(3)有同学提出检验火柴头中KClO3的另一实验方案:
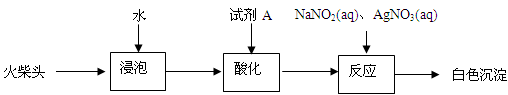
试剂A为???????????????,加入NaNO2的目的是???????????????????????????。
(4)设计实验:简述验证滤渣D中含有MnO2的一个实验方案,并写出有关反应的化学方程式。??????????????????????????????????????????????????????????????????????????????????。
参考答案:(1)KMnO4溶液褪色或颜色变浅或其他正确描述(2分)、<
本题解析:
试题分析:(1)若有硫元素燃烧中生成了二氧化硫气体会使KMnO4溶液褪色或颜色变浅。用针筒主是使燃烧产生的气体顺利进入试管。
(2)氯元素燃烧中主要生成了氯化氢气体,只要取少量滤液C置于试管中,先后加入HNO3、AgNO3溶液,若观察到白色沉淀产生,,即可证明火柴头中含有氯元素。相当于是氯离子的检验。
(3)KClO3有强的氧化性,在酸性环境下,如加硝酸或HNO3主要是酸化,而亚硝酸钠有较强的还原性,可以还原KClO3为氯离子。
(4)验证是否有MnO2,可以用实验室制取氯气的方法,也可以做为催剂如取少量滤渣D加入装有少量H2O2的试管中,有大量气泡放出说明含有MnO2,相关反应?? 2H2O2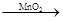 2H2O+O2↑
2H2O+O2↑
本题难度:一般
4、实验题 (共8分)某化学研究性学习小组以海带为原料制取了少量碘水。现用四氯化碳从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50 mL碘水和15 mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
C.检查分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转分液漏斗,振荡,并不时旋开活塞放气,最后关闭活塞,分液漏斗放正;
(E)旋开活塞,用烧杯承接溶液;
(F)从分液漏斗上口倒出上层水溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置、分层;??????????????????????????
就此实验,完成下列填空:
(1)正确操作步骤的顺序是:(用上述各操作的编号字母填写) → → →A→G→ →E→F。
(2)能选用四氯化碳从碘水中萃取碘的原因是??????????????????????;?_________________________。
(3)已知碘在酒精中的溶解度比在水中大的多,能不能用酒精来萃取碘水中的碘?????(填“能”或“不能”),其理由是 ???????? 。
参考答案:(1)? C → B → D →A→G→ H →E→F<
本题解析:略
本题难度:一般
5、选择题 下列关于0.2mol/L的Ba(NO3)2溶液不正确的说法是
A.500mL溶液中NO3-物质的量为0.2NA
B.500mL溶液中NO3-离子浓度为0.4mol/L
C.500mL溶液中Ba2+离子浓度为0.2mol/L
D.1L溶液中阴、阳离子总数为0.8NA
参考答案:AD
本题解析:分析:A、根据n(NO3-)=2c(Ba(NO3)2)V计算;
B、根据溶液中离子的物质的量浓度=化学式中离子个数×溶液的物质的量浓度计算;
C、根据溶液中离子的物质的量浓度=化学式中离子个数×溶液的物质的量浓度计算;
D、根据N=化学式中阴阳离子个数×c(Ba(NO3)2)VNA计算.
解答:A、n(NO3-)=2 c(Ba(NO3)2)V=2×0.2mol/L×0.5L=0.2mol,故A错误;
B、C(NO3-)=2×c(Ba(NO3)2)=2×0.2mol/L=0.4mol/L,故B正确;
C、C(Ba2+)=1×c(Ba(NO3)2)=1×0.2mol/L=0.2mol/L,故C正确;
D、N(阴阳离子数)=3×c(Ba(NO3)2)V NA=3×0.2mol/L×1L×NA=0.6NA,故D错误;
故选AD.
点评:本题考查了有关物质的量浓度的计算,难度不大,明确化学式与离子的关系是解本题的关键.
本题难度:困难