��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����£�Ksp��CaSO4��=9?10��6��������CaSO4��ˮ�еij����ܽ�ƽ������ͼ������˵����ȷ����?????
 ????????????????????????????????
????????????????????????????????
A�����κ���Һ�У�c(Ca2+)��c(SO42��)�����
B��b�㽫�г������ɣ�ƽ��� ��Һ��c(SO42��)һ������3?10��3 mol��L��1
��Һ��c(SO42��)һ������3?10��3 mol��L��1
C��a���Ӧ��Ksp����c���Ӧ��Ksp
D��d����Һͨ���������Ա䵽c��
�ο��𰸣�C
�����������
�����Ѷȣ���
2��ѡ���� ��4molA�����2molB��������2L���ܱ������У���Ϻ������·�Ӧ�� 2A(g) + B(g) == 2C (g) ������2s����C��Ũ��Ϊ 0.6mol/L ������˵����ȷ���� [???? ]
A��������A��ʾ�ķ�Ӧ����Ϊ0.6mol/��L��s��
B��������B��ʾ�ķ�Ӧ����Ϊ0.3mol/��L��s��
C��2sʱ����A��ת����Ϊ30��
D��2sʱ����B��Ũ��Ϊ0.3mol/L
�ο��𰸣�C
���������
�����Ѷȣ�һ��
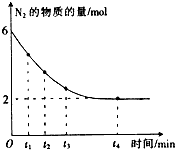
3��ѡ���� һ�������£����ܱ������н��еĿ��淴Ӧ��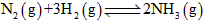 ��N2�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ��ʾ�������淴Ӧ��������ʱ����
��N2�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ��ʾ�������淴Ӧ��������ʱ����
 [???? ]
[???? ]
A��t1
B��t2
C��t3
D��t4
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ������CuO��CO�з������·�Ӧ��CuO��s����CO��g�� Cu��s����CO2��g������֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
Cu��s����CO2��g������֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
�¶�/��
| 1 000
| 1 150
| 1 300
|
ƽ�ⳣ��
| 4��0
| 3��7
| 3��5
��ش��������⣺
��1���÷�Ӧ��ƽ�ⳣ������ʽK��________����H________0���>����<����������
��2����һ���ݻ�Ϊ10 L���ܱ������У�1 000 ��ʱ����Cu��CuO��CO��CO2��1��0 mol����Ӧ����10 min��ﵽƽ�⡣���ʱ�䷶Χ�ڷ�Ӧ��ƽ����Ӧ����v��CO2����________��CO��ƽ��ת���ʣ�________��
��3������ߣ�2����CO��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��__??????? __��
A������Cu��������B������CuO����? C���Ƴ�����CO2????? D����߷�Ӧ�¶�
E����С�������ݻ�?? F��������ʵĴ���
�ο��𰸣���1�� c(CO2)��c(CO) ��?������2��0.006
�����������1��ƽ�ⳣ������һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը÷�Ӧ��ƽ�ⳣ������ʽK��c(CO2)��c(CO)�����ݱ������ݿ�֪�������¶�ƽ�ⳣ���Ǽ�С�ģ���˵������Ӧһ���Ƿ��ȷ�Ӧ��
��2��������CO�����ʵ�����x��������CO2��x������ƽ��ʱ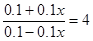 �����x��0.6mol������CO2�ķ�Ӧ������ �����x��0.6mol������CO2�ķ�Ӧ������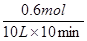 ��0.006 mol/(L��min)��CO��ƽ��ת���ʣ�0.6��1.0��0.6�� ��0.006 mol/(L��min)��CO��ƽ��ת���ʣ�0.6��1.0��0.6��
��3����������Ӧ�Ƿ��ȵġ��������Ŀ��淴Ӧ�����Խ���CO2��Ũ��ƽ��������Ӧ�����ƶ���CO��ת����������ģ�ѡ��C��ȷ���ı�����������ƽ�ⲻ�ƶ���AB����ȷ�������¶�ƽ�����淴Ӧ�����ƶ���ת���ʽ��ͣ�D����ȷ�ı�ѹǿ��ʹ�ô�����ƽ�ⶼ�Dz��ƶ��ģ�������ȷ�Ĵ�ѡC��
�����Ѷȣ�һ��
5������� ��10�֣�
��.��һ�������£��ݻ�Ϊ 100 L�ܱ������з�����Ӧ��CH4(g)+H2O(g) 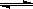 CO(g)+3H2(g)����H>0 CO(g)+3H2(g)����H>0
��1.0 mol CH4��2.0 mol H2O(g)ͨ����ܱ����� l0 minʱ��0.1 mol CO���ɣ���10 min�ڸ÷�Ӧ��ƽ������v(H2)????????????????????????��
��.��ѹǿΪ0.1 MPa������,�ݻ�ΪV Lij�ܱ�������a mol CO�� 2a mol H2�ڴ��������·�Ӧ���ɼ״���CO(g)+2H2(g)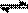 CH3OH(g)��CO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ�� CH3OH(g)��CO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��

�ٸ÷�Ӧ�ġ�H????0 (�<������>����=��)��
��100��ʱ�÷�Ӧ��ƽ�ⳣ��K=???????????????���ú�a��V�Ĵ���ʽ��ʾ����
�����¶��ݻ����������£�����ܱ�����������a mol CO�� 2a mol H2���ﵽ��ƽ��ʱ��CO��ת������?�������������С�����䡱����ƽ�ⳣ����?�������������С�����䡱����
�ο��𰸣�(1)? 0��0003 mo1��L��1��min��1
(
�����������1��CH4(g)+H2O(g) 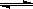 CO(g)+3H2(g) CO(g)+3H2(g)
��ʼ? 1???? 2
ת��?????????????????? 0.1??? 0.3
����v(H2)=0.3mol��100L��10min=0��0003 mo1��L��1��min��1
��2������ͼ��֪�������¶ȵ����ߣ�COת�������ͣ�����ƽ��������У����Է�ӦΪ���ȷ�Ӧ
��??? CO(g)+2H2(g)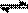 CH3OH(g) CH3OH(g)
��ʼ?? a???? 2a
ת��? 0.5 a?? 1a???????? 0.5 a
ƽ��? 0.5a??? a????????? 0.5a
K=��0.5a��V����(a/v)2����0.5a��V��=" V" 2��a2
�����õ�Чƽ��ԭ����������䣬��ƽ�������ƶ���COת����������Ϊ�¶�û��ƽ�ⳣ�����䡣
�����Ѷȣ�һ��
|