微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 同温同压下,甲容器中CH4与乙容器中C2H2 ,C2H4 混合气体的体积相等,则甲、乙两个容器中原子总数之比不可
,C2H4 混合气体的体积相等,则甲、乙两个容器中原子总数之比不可 能是(???????)
能是(???????)
A.10:9
B. 10:11
C. 5:6
D. 1:1
参考答案:C
本题解析:略
本题难度:一般
2、计算题 将6.50g锌投入200mL某浓度的盐酸溶液中,锌和盐酸恰好完全反应。计算:
⑴6.50g锌的物质的量
⑵所用盐酸中HCl的物质的量浓度
⑶反应后生成的H2在标准状况下的体积
参考答案:(1)0.1mol ????(2)CHCl="1mol/L"
本题解析:
试题分析:(1)n(Zn)=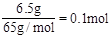 。
。
(2)根据Zn与盐酸反应的方程式可知参加反应的盐酸为0.2mol,所以c(HCl)=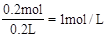 本题难度:一般
本题难度:一般
3、选择题 有一种pH为12的NaOH溶液100 mL,要使它的pH降到11,
(1)如果加入蒸馏水,应加??????????????mL;(提示:溶液总体积具有加和性。下同)
(2)如果加入pH=lO的NaOH溶液,应加_______???mL;
(3)如果加入O.Ol mol・L-1的盐酸,应加_______ mL。
参考答案:(共6分)(1)900 (2分) (2)1000?(2分)(
本题解析:略
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数,下列叙述中正确的是(??)
A.0.1mol・L-1稀硫酸中含有硫酸根离子个数为0.1NA
B.1molCH3+(碳正离子)中含有电子数为10NA
C.标准状况下,0.5NA个NO和0.5NA个O2混合气体的体积约为22.4 L
D.12.4g白磷中含有磷原子数为0.4NA
参考答案:D
本题解析:
试题分析:注意物质的量相关计算公式的熟练应用。
A中考查物质的量浓度概念,由N=n×NA和n = C×V可得,光由已知浓度不能确定溶液中微粒个数,应该还要给出溶液的体积才可以计算,所以A错误;B,要先求出一个CH3+中电子数为6+3-1=8个,所以1molCH3+(碳正离子)中含有电子数为8NA;C中标准状况下, NO和O2混合会发生反应2NO+ O2==2NO2,所以气体的体积不是22.4 L,应为0.75×22.4 L,C错误;D中白磷分子为P4,12.4g白磷的物质的量为0.1mol,
本题难度:一般
5、选择题 下列说法中正确的是( )
A.将0.1molCuSO4?5H2O晶体加入到100mL水中,该溶液物质的量浓度为1mol?L-1
B.一定体积的浓硫酸(其中含0.2molH2SO4)与足量的铜共热反应,生成SO2气体0.1mol
C.将34.2gAl2(SO4)3溶于水配成100mL溶液[Al2(SO4)3的相对质量为342J,取出10mL该溶液中Al3+浓度为1mol?L-1
D.KCl溶液的密度为1.174g?cm-3,物质的量浓度为4.0mol?L-1,则此溶液中KCl的质量分数为
74.5×4.0
1.174×1000
×100%
参考答案:A.将0.1molCuSO4?5H2O晶体溶于水配成100m
本题解析:
本题难度:一般
|