微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某工厂废弃的钒渣中主要含V2O5、VOSO4、K2SO4、SiO2等,现从该钒渣回收V2O5的工艺流程示意图如下:
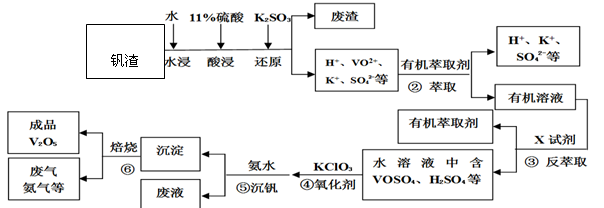
(已知:沉淀为(NH4)2V6O16,全钒液流储能电池是利用不同价态离子对氧化还原反应来实现化学能和电能相互转化的装置,②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂)。
R2(SO4)n(水层)+2nHA(有机层) 2RAn(有机层) + nH2SO4(水层)
2RAn(有机层) + nH2SO4(水层)
回答下列问题:
(1)(NH4)2V6O16中钒(V)的化合价为 ,①中产生的废渣的主要成分是 。
(2)工艺中反萃取所用的X试剂为 。
(3)为提高②中萃取效率,应采取的措施是 。
(4)请完成④中的反应离子方程式:
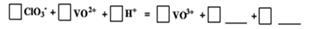
(5)成品V2O5可通过铝热反应来制取金属钒,写出该反应的化学方程式: 。
(6)将两个全钒液流储能电池串联后作为电源,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,装置如下:
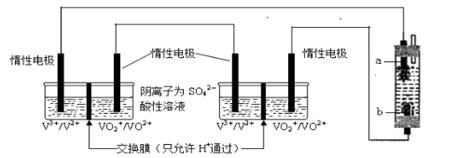
b为电解池的 极,全钒液流储能电池正极的电极反应式为 ;
若通过消毒液发生器的电子为0.2 mol,则消毒液发生器中理论上最多能产生 gNaClO。
参考答案:(除标记外每空2分,共15分)
(1)+5
本题解析:
试题分析:(1)根据化合物中正负化合价代数和为0可判断(NH4)2V6O16中N为-3、H为+1、O为-2价,则钒(V)的化合价为+5价;根据流程图可知,只有二氧化硅不溶于硫酸,所以废渣的主要成分是SiO2;
(2)从流程图中可看出,加入反萃取剂X后,又得到有机萃取剂和含V元素的混合液,根据R2(SO4)n(水层)+2nHA(有机层) 2RAn(有机层) + nH2SO4(水层)可知,该平衡应逆向进行,所以加入的X是硫酸;
2RAn(有机层) + nH2SO4(水层)可知,该平衡应逆向进行,所以加入的X是硫酸;
(3)为提高②中萃取效率,使上述平衡正向移动,则应加入碱性物质,同时多次萃取也可增大萃取效率;
(4)V元素的化合价从+4价升高到+5价,则氯酸根离子中的Cl元素的化合价从+5价应降低到-1价,同时根据元素守恒,则产物中还有水生成,所以产物的空白为Cl-和H2O;再根据得失电子守恒,VO2+和VO3+的系数是6,氯酸根离子和氯离子的系数是1,根据电荷守恒,则氢离子的系数是6,水的系数是3;
(5)铝热反应是单质Al与金属氧化物的置换反应,所以用Al与五氧化二钒反应生成氧化铝和钒的化学方程式是10Al+3V2O5 6V+5Al2O3;
6V+5Al2O3;
(6)电解饱和食盐水时,氯气在阳极产生,氢氧化钠再阴极产生,若使氯气被全部吸收,则氯气在下端,所以b极产生氯气,则b极为阳极;全钒液流储能电池正极发生还原反应,V元素的化合价降低,与b相连的为正极,所以正极反应式是VO2++ e-+2H+=VO2++H2O;产生氯气的电极反应式为2Cl--2e-=Cl2↑,氯气与氢氧化钠反应的离子方程式是Cl2+2 OH-= Cl-+ ClO-+H2O,当电路中通过0.2mol电子时,产生氯气的物质的量是0.1mol,则消毒液发生器中理论上最多能产生0.1molNaClO,其质量是7.45g。
考点:考查对流程的分析,元素化合价的判断,电化学反应原理的应用
本题难度:困难
2、选择题 如图是工业上采用离子交换膜法电解足量饱和食盐水的示意图。下列有关说法中不正确的是:?????????????????????

A.从E口逸出的是氢气
B.向B口中加入含少量NaOH 的溶液以增强导电性
C.标准状况下每生成22.4LCl2,便产生2molNaOH
D.向电解后的阳极室溶液中加入适量盐酸,各物质可以恢复到电解前的浓度
参考答案:D
本题解析:略
本题难度:一般
3、选择题 电解含有重水(D2O)的普通水时,在两极共收集到气体18.5g,其体积恰好是33.6L(标准状况).这些气体中普通氢和重氢(D)的原子个数比为( )
A.1:1
B.2:1
C.3:1
D.4:1
参考答案:电解水的方程式为2H2O
本题解析:
本题难度:一般
4、选择题 用惰性电极电解饱和Na2SO4溶液,若保持温度不变,则一段时间后( )
A.溶液pH变大
B.c(Na+)与c(SO42-)的比值变大
C.溶液浓度变大,有晶体析出
D.溶液浓度不变,有晶体析出
参考答案:A.硫酸钠是强酸强碱盐,其水溶液呈中性,用惰性电极电解饱和硫
本题解析:
本题难度:简单
5、选择题 在一定温度下,用铂电极电解饱和Na2SO4溶液,对电解质溶液判断正确的是
A.不会有晶体析出
B.浓度变大
C.浓度变小
D.pH不变
参考答案:D
本题解析:电解Na2SO4溶液,实质是电解水,故水量减少,饱和Na2SO4溶液要析出晶体,但因其是饱和溶液,故其浓度不变。
本题难度:简单