微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 检验盐溶液中是否含有某种离子,下列方法正确的是?????????????????
A.加入AgNO3溶液,有白色沉淀生成,则证明含有Cl-
B.加入BaCl2溶液,产生白色沉淀,则证明有SO42-
C.加入盐酸,放出能使澄清石灰水变浑浊的气体,则证明有CO32-
D.加浓NaOH溶液后加热,有使湿润的红色石蕊试纸变蓝的气体产生,则证明有NH4+
参考答案:D?
本题解析:A.加入AgNO3溶液,有白色沉淀生成,可能含有Cl-、SO42-、CO32-等。
B.加入BaCl2溶液,产生白色沉淀,可能含有SO42-、CO32-、Ag+等。
C.加入盐酸,放出能使澄清石灰水变浑浊的气体,可能有CO32-、HCO3-、SO32-、HSO3-等。
本题难度:一般
2、实验题 “白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
方案一:取三块镀锌铁皮(A.B.C,截自同一块镀锌铁皮),将镀锌铁皮A放入烧杯中,加入40mL
6mol・L-1盐酸,反应时用玻璃棒小心翻动镀锌铁皮,待锌镀层反应完全时,立即将未反应的铁皮取出,洗涤.小心烘干.称量。将B.C重复上面的实验。
(1)锌镀层完全反应的标志是________________________________
(2)如何检验铁片已经洗净?________________________________
方案二:已知锌与强碱溶液反应的离子方程式为:Zn+2OH-+2H2O=[Zn(OH)4]2-+H2↑。某同学按下图装置设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为Scm2.质量为mg的镀锌铁皮放入
6mol・L-1 NaOH溶液中。回答下列问题:
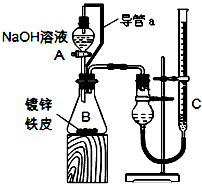
(3)装置中导管a的作用是________________________________
(4)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②待B中不再有气体产生并恢复至室温;
③由A向B中滴加足量NaOH溶液;④上下移动C,使干燥管和C中液面相平。
上述操作的顺序是__________________(填序号)。
参考答案:(1)反应速率突然减小
(2)取最后一次洗出液,滴加A
本题解析:
本题难度:困难
3、简答题 某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧.他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.
(1)通过钠在CO2气体中燃烧的实验,你认为燃烧的条件是______.
(2)燃烧的本质是______.
(3)2010年8月初发生的俄罗斯森林大火有比伦敦市还要大的面积.控制森林火灾是世界性难题.根据燃烧的条件,请你解释为什么设置森林防火隔离带能有效阻止森林火灾的蔓延?______.
【提出假设】假设1:白色物质是Na2O.
假设2:白色物质是Na2CO3.
假设3:白色物质是Na2O和Na2CO3的混合物.
【设计实验方案.验证假设】该小组对燃烧后的白色产物进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 结论
方案1
取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液
溶液变成红色
白色物质为Na2O
|
方案2
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液
出现白色沉淀 |
③静置片刻,取上层清液于试管中,滴加无色酚酞试液
无明显现象
【思考与交流】
(4)甲同学认为方案1得到的结论不正确,其理由是______.
(5)乙同学认为方案2得到的结论正确,白色物质为______.
(6)通过方案1和方案2的实验,你认为上述三个假设中,______成立.你的理由是______.
(7)钠在二氧化碳中燃烧的化学方程式为______.
(8)丙同学认为白色物质有可能是氢氧化钠.你是否同意丙同学的观点,并简述理由:______.
参考答案:(1)物质燃烧依据钠在二氧化碳中的燃烧分析需要物质本身能燃烧
本题解析:
本题难度:一般
4、填空题 某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
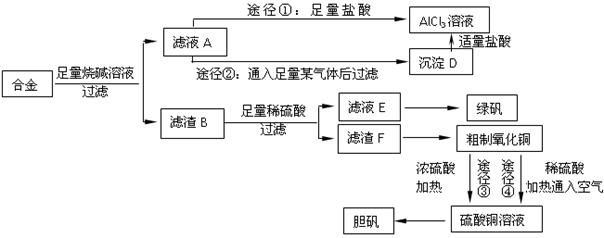
回答下列问题:
(1)写出合金与烧碱溶液反应的离子方程式????????????????????????????,有人认为合金与烧碱溶液形成了原电池,则作为原电池负极的物质是???????????。
(2)由滤液A制AlCl3溶液的途径有①和②两种,你认为合理的是??????????????????????。上述实验方案多处采用了过滤操作,过滤所用到的玻璃仪器有????????????????????和玻璃棒;其中玻璃棒的作用是?????????????????。
(3)用粗制氧化铜通过两种途径制取胆矾,与途径③相比,途径④明显具有的两个优点是:????????????????????????????、????????????????????????????????????。
(4)通过途径④实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、?????????????????????、冷却结晶、?????、自然干燥。其中“加热通氧气”所起的作用为??????????????????? 91exam.org??????????????????????????(用离子方程式表示)。
(5)在测定所得胆矾(CuSO4・xH2O)中结晶水x值的实验过程中:称量操作至少进行????次。若测定结果x值偏高,可能的原因是?????????。
a.加热温度过高?? b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却???????????? d.胆矾晶体部分风化????????????
e.加热时胆矾晶体飞溅出来?????????? f.所用坩埚事先未干燥(潮湿)
参考答案:(1)2Al+2OH-+6H2O=2[Al(OH)4]-+3
本题解析:略
本题难度:一般
5、选择题 实验是研究化学的基础,下图中所示的实验方法、装置或操作完全不正确的是(??? )
A.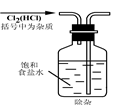 B? B?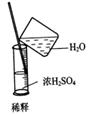 ?C ?C ??? D. ??? D.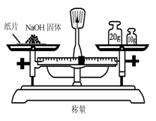
参考答案:ABD
本题解析:
试题分析:A、该操作会造成食盐水倒吸。
B、浓硫酸稀释的正确做法是将浓硫酸倒进水中。
D、用天平称量物品时,要注意是“左物右码”,因为NaOH有很强的吸湿性,很容易吸收空气中的水蒸气而潮解,直接暴露在空气中称量的话会造成误差除此外,还因为NaOH会和空气中的二氧化碳反应,生成NaCO3,降低样品的纯度,所以,可以用称量瓶来称量。
点评:此题考核了常见实验操作方法,要求学生平时的实验操作动作要规范,正确。
本题难度:简单
|