微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)高温下,炼铁高炉中存在下列平衡:
回答下列问题:
(1)写出该反应的平衡常数表达式_______________________________________。
(2)升高温度,该反应的平衡常数K值将__________(填“增大”、“减小”、“不变”),平衡体系中固体的质量将__________(填“增大”、“减小”、“不变”)。
(3)已知11OO℃时该反应的平衡常数K=0.263。在1100℃时,测得高炉中。
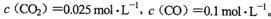 此时该的化学反应速度是v(正)___________(填“>”、“<”、“=”)v(逆),原因是_________________________________________________________________________。
此时该的化学反应速度是v(正)___________(填“>”、“<”、“=”)v(逆),原因是_________________________________________________________________________。
(4)保持高炉温度为1100℃,向高炉中补充大量的空气,重新达到平衡后,该反应的平衡常数K值 __________(填”>”、“<”、“=”)0.263。
参考答案:(1)K= 本题解析:
本题解析:
试题分析:(1)FeO(s)+CO(g)?Fe(s)+CO2(g)的平衡常数K= ;
;
(2)该反应是吸热反应,升高温度,化学平衡正向移动,该反应的平衡常数K值将增大,生成的固体铁的质量会比原来氧化亚铁的质量少;
(3)因为此时Q=0.025/0.1=0.25<K=0.263,反应没有处于平衡状态,反应是向正反应方向进行的,因此正反应速率大于逆反应速率。(4)K只受温度影响,温度不变,K不变,等于0.263。
考点:考查化学平衡常数,化学反应速率等知识。
本题难度:一般
2、选择题 用来表示可逆反应:2A(g)+B(g) 2C(g)(正反应为吸热反应)的正确图像是 [???? ]
2C(g)(正反应为吸热反应)的正确图像是 [???? ]
A.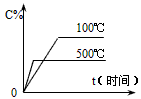
B.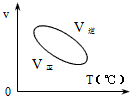
C.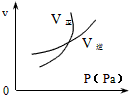
D.
参考答案:C
本题解析:
本题难度:一般
3、实验题 (共12分)
(1)在某容积不变的密闭容器中,有可逆反应:mA(g)+nB(g) pC(g)+qD(S)△H<0如图某反应过程中各物质物质的量n(mol)随时间t的变化曲线图。
pC(g)+qD(S)△H<0如图某反应过程中各物质物质的量n(mol)随时间t的变化曲线图。
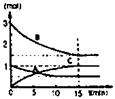
①该反应的平衡常数表达式为(各物质浓度的指数用数值表示):???。
②若充入A,K值???(填一定增大、一定减小、或可能增大也可能减小、不变);正反应速率____(填增大、减小、不变)。
③若体积为10升的密闭容器中,500℃、有催化剂存在的条件下,根据图示回答下列问题:在0~15min内的平均反应速率:v(B)=?????????????
(2)对于某可逆反应:A(g)+B(g) 2C(g) △H<0。若该反应的正反应速率与时间的关系如图所示。在其它条件不变的情况下,请填空:
2C(g) △H<0。若该反应的正反应速率与时间的关系如图所示。在其它条件不变的情况下,请填空:

①写出t2时改变的条件可能是:???????(用文字表达);
②t4时改交的条件可能是????(用编号表示,多选扣分)
A.增大压强????????? B.减小压强
C.使用催化剂???????? D.升高温度
E.增大A的浓度
参考答案:①K= 本题解析:
本题解析:
试题分析:(1)?反应平衡常数K值只与温度有关,与反应物浓度无关。其他条件相同时,
增大反应物浓度反应速率增大。?计算平均反应速率,以反应物B为例:V(B)=1.5mol/15min
×10L???? (2)?在t2时反应速率骤降,温度降低,分子运动速率减慢,反应速度也减慢。
?影响反应速率的因素有温度、浓度、压强、催化剂,在t4时反应速率升高,对于有气体
参与的化学反应,其他条件不变时(除体积),增大压强,即体积减小,反应物浓度增大,
速率增加。正催化剂能使反应速率
本题难度:一般
4、选择题 下列说法正确的是
A.可逆反应的特征是正反应速率和逆反应速率相等
B.对已达到化学平衡的反应仅改变浓度,若平衡移动,则平衡常数(K)一定不变。
C.电镀时应把镀件置放电解槽的阳极。
D.电解AlCl3来制取金属铝。
参考答案:B
本题解析:A 错误,可逆反应的特征是在相同条件下既能向正反应方向进行,又能向逆反应方向进行
B 正确,平衡常数(K)只跟温度有关,温度不变,平衡常数(K)不变
C 错误,电镀时应把镀件置放电解槽的阴极
D 错误,电解熔融的氧化铝来制取金属铝
本题难度:一般
5、选择题 对于可逆反应:mA(g)+nB(g)  xC(g) ΔH,在不同温度及压强(P1、P2)条件下,反应物A的转化率如图所示,下列判断正确的是
xC(g) ΔH,在不同温度及压强(P1、P2)条件下,反应物A的转化率如图所示,下列判断正确的是
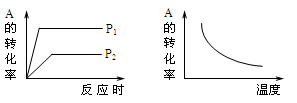
A.ΔH<0,m+n>x
B.ΔH>0,m+n<x
C.ΔH<0,m+n<x
D.ΔH>0,m+n>x
参考答案:A
本题解析:
试题分析:由压强对平衡的影响图像可以看出,P1条件下反应先达平衡,P1>P2 ,压强增大,A的转化率增大,平衡向正方向移动,m+n>x ,温度升高,A的转化率减小,平衡向逆反应方向移动,正反应放热,ΔH<0,答案选A。
考点:化学平衡的图像
本题难度:一般