微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设阿伏加德罗常数的值为NA,则下列说法正确的是
A.常温常压下,18.0g NH4+中所含的质子数为10 NA
B.111g CaCl2晶体中所含共用电子对的数目为2NA
C.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA
D.室温下,8 g甲烷含有共价键数为2NA
参考答案:D
本题解析:A错,常温常压下,18.0g NH4+中所含的质子数为11 NA;B错,2晶体为离子晶体,不存在共用电子对;C错,常温下,铝遇冷的浓硫酸会发生钝化;D正确;
本题难度:一般
2、选择题 质量相等的下列气体中,分别放到同体积的密封容器中,同温下,压强最大的是( )
A.H2
B.O2
C.C2H2
D.N2
参考答案:A
本题解析:同质量、同体积、同温下,压强与摩尔质量成反比,M(H2)最小,故压强最大。本题考查阿伏加德罗定律的应用。
本题难度:一般
3、选择题 假设R元素无同位素,元素R原子的质量数为A,Rm-的核外电子数为x,则W g Rm-离子所含中子的物质的量为
A.(A-x+m)mol
B.(A-x-m)mol
C.W/A(A-x+m)mol
D.W/A(A-x-m)mol
参考答案:C
本题解析:
试题分析:Rm-的核外电子数为x,则R的原子序数是x-m。因此R的中子数是a-x+m,所以W g Rm-离子所含中子的物质的量为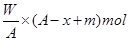 ,答案选C。
,答案选C。
点评:在计算有关原子的组成时,需要掌握几个关系式,即质子数+中子数=质量数、质子数=核外电子数=原子序数=核电荷数。
本题难度:一般
4、选择题 质量分数为n的NaOH溶液,其物质的量浓度为amol/L,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为bmol/L,则a与b的关系正确的是( )
A.b>2a
B.b<2a
C.b=2a
D.a=2b
参考答案:令质量分数为n的NaOH溶液的密度为xg/ml,质量分数为2
本题解析:
本题难度:简单
5、选择题 用胆矾(CuSO4-5H2O)晶体配制1mol/L的CuSO4溶液500mL,下列方法正确的是( )
A.称取80g胆矾使其溶于500mL水中
B.称取125g胆矾使其溶于500mL水中
C.称取80g胆矾使其溶于375g水中
D.称取125g胆矾使其溶于适量水中,再加水稀释至500mL
参考答案:用胆矾(CuSO4-5H2O)晶体配制1mol/L的CuSO
本题解析:
本题难度:简单