微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某同学探究SO2有关性质。
(1)将SO2通入BaCl2溶液中,将所得溶液分成2份,在第一份中加入NaOH溶液,在第二份中滴入FeCl3溶液,两份都有白色沉淀。BaCl2溶液中通入SO2气体的现象为???。在第二份溶液中滴入FeCl3溶液时,SO2表现???性,反应的离子方程式为???????????????????,生成沉淀的化学式为???????。
(2)下列不能用来吸收SO2气体的是????。
A.KMnO4(aq)
B.过量氨水
C.石灰水
D.盐酸
(3)工业废气含SO2为7%(体积分数),在同温同压下,将以上废气用废气中的O2氧化含SO3。反应后气体体积为原来气体的96.64%。则SO2的转化率为????。
(4)硫原子33 16S的电子排布式为???????。
参考答案:(1)无明显现象。???还原性,?? 2Fe3++H2SO3
本题解析:
试题分析:(1)根据复分解反应发生的条件,由于酸性HCl>H2SO3?故SO2通入BaCl2溶液中不会与溶质发生反应,只与水反应生成H2SO3?故得到BaCl2、H2SO3混合液。再加入NaOH溶液时发生反应2NaOH+H2SO3=Na2SO3+H2O, Na2SO3和BaCl2发生离子反应生成BaSO3白色沉淀。另一份滴入FeCl3溶液,则发生氧化还原反应:2FeCl3+SO2+2H2O=2FeCl2+2HCl+H2SO4 , BaCl2与H2SO4生成 BaSO4白色沉淀。在该反应中SO
本题难度:一般
2、实验题 硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
[甲方案]:如右图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。
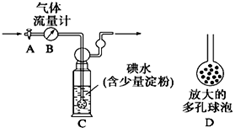
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是___________________________________。
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量_________(填“偏高”、“偏低”或“无影响”)。
[乙方案]:实验步骤如下面流程图所示:
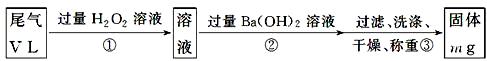
(3)步骤①中过量H2O2的作用是?????????????????????????????????????????????????????
(4)写出步骤②中反应的化学方程式______________________________________
(5)步骤②中Ba(OH)2是否足量的判断方法是_______________________________
___________________________________________________________________。
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为_____________________________(用含有V、m的代数式表示)。
参考答案:(1)增大气体与溶液的接触面积,有利于SO2与碘水反应
本题解析:
试题分析:甲方案利用的原理为:SO2+I2+2H2O=H2SO4+2HI,最后测定剩余气体的体积,进而定尾气中二氧化硫的含量;
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以增大SO2与碘水的接触面积,使SO2和碘水充分反应;
故答案为:增大SO2与碘水的接触面积,使SO2和碘水充分反应;
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,则通入尾气的体积增大,因此SO2含量偏低;
故答案为:偏低;
乙方案利用的原理为:SO2+H2O2=H2SO4,H2SO4+B
本题难度:困难
3、选择题 下列实验用来证明SO2的存在,其中正确的是
①能使品红溶液褪色②能使湿润的蓝色石蕊试纸变红③能使澄清的石灰水变浑浊④通入足量的NaOH溶液中,再滴入BaCl2溶液,有白色沉淀生成,该沉淀溶于盐酸⑤通入溴水能使溴水褪色,再滴入Ba(NO3)2溶液,有白色沉淀生成
A.都能证明
B.都不能证明
C.①⑤能证明
D.只有⑤能证明
参考答案:D
本题解析:①错,能使品红溶液褪色的气体有二氧化硫或氯气等气体;②错,能使湿润的蓝色石蕊试纸变红的气体除二氧化硫外还可以是HCL气体等;③错,能使澄清的石灰水变浑浊的气体可以是二氧化硫或二氧化碳气体;④通入足量的NaOH溶液中,再滴入BaCl2溶液,有白色沉淀生成,该沉淀溶于盐酸的气体可以是二氧化硫或二氧化碳气体;⑤正确;
本题难度:一般
4、选择题 某气体通入品红溶液中,溶液褪色.加热后又恢复为原来颜色.该气体是
A.SO2
B.NO2
C.CO2
D.Cl2
参考答案:A
本题解析:分析:二氧化硫具有漂白性,是因利用化合反应生成暂时稳定的无色化合物,加热时该化合物分解,品红又恢复成红色.
解答:A.SO2是一种漂白剂,能使品红褪色,但是生成的无色物质不稳定,加热时该化合物分解,二氧化硫从溶液中逸出,因此品红溶液又恢复原来颜色,故A正确;
B.NO2不是漂白剂,通入品红溶液中,溶液不褪色,故B错误;
C.CO2不是漂白剂,通入品红溶液中,溶液不褪色,故C错误;
D.Cl2与水反应生成次氯酸,次氯酸是一种漂白剂,能使品红褪色,加热后颜色不变,故D错误;
故选A.
点评:本题主要考查了物质的漂白性,难度不大,注意区分.
本题难度:一般
5、填空题 二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2+11O2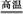 8SO2+2Fe2O3,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为 L。?
8SO2+2Fe2O3,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为 L。?
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率。(已知SO3熔点为16.8 ℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响。)
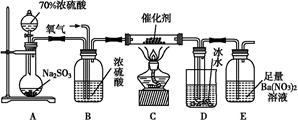
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是?????????????????????????。
②实验过程中,需要通入氧气。试写出一个用如图所示装置制取氧气的化学方程式??????????????????????????????。
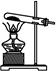
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是???????????。
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是 (用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如图装置验证二氧化硫的化学性质。
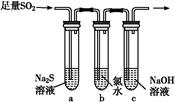
①能说明二氧化硫具有氧化性的实验现象为??????????????????????????????。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是 (填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为?????????????????????????????????????????????????????。
③当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)= (用含硫微粒浓度的代数式表示)。
参考答案:(1)S、Fe 11.2
(2)①打开分液漏斗上的活塞
本题解析:(1)4FeS2+11O2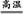 8SO2+2Fe2O3,该反应中被氧化的元素是S、Fe;设生成二氧化硫的体积是x L。
8SO2+2Fe2O3,该反应中被氧化的元素是S、Fe;设生成二氧化硫的体积是x L。
4FeS2+11O2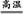 本题难度:一般
本题难度:一般