��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� һ���¶��£�����������������Һһ�������Ե���
A���������Al��Ӧ�ų�H2����Һ
B���ӷ�̪������ɫ����Һ
C��pH=6����Һ
D��c(H��)>c(OH��)������ˮ��Һ
�ο��𰸣�D
���������
���������A���������ܺ��ᷴӦҲ�ܺͼӦ�������������Բ�ѡA��B�������̪������ɫ����ҺҲ���������ԵĻ������Եģ����Բ�ѡB��C��û��˵����Һ���¶ȣ�����ȷ����Һ�������Ӻ�����������Ũ��֮��Ĺ�ϵ����ѡC��D����������Ũ�ȴ�������������Ũ��ʱ����Һ�����ԣ�ѡD��
���㣺��Һ������ԡ�
�����Ѷȣ�һ��
2��ѡ���� ����ʱ����0.10 mol/L��NaOH��Һ����20.0 mLδ֪Ũ�ȵ�ijһԪ��HA��Һ�У���ҺpH�����NaOH��Һ����仯������ͼ�������й�˵������ȷ����
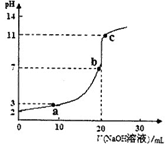
A����һԪ����ҺŨ��Ϊ0.10mol/L
B��a��b��c���ˮ��Һ������������ǿ
C������ʱ��HA�ĵ��볣��Ka l��10-5
l��10-5
D��a���c����ʾ��Һ��H2O�ĵ���̶���ͬ
�ο��𰸣�C
���������
���������A.NaOH��HA��һԪ�һԪ�ᣬ������ǡ����ȫ��Ӧʱ���ߵ����ʵ�����ȣ����Ҳ��ȣ�˵�����ǵ�Ũ����ȣ���һԪ����ҺŨ��Ҳ��ȣ�Ϊ0.10mol/L����ȷ��B.��������Һ�м���ǿ��NaOH�������кͷ�Ӧ�����Σ������ƶ�������Ũ��������Һ�ĵ�������ǿ��������������ȫ��Ӧʱ�������ƶ����ӽ�һ�����࣬����Ũ��������Һ�ĵ�������ǿ�����ڼ���NaOH�����൱������NaA��Һ�м���NaOH��Һ����Һ�������ƶ�����Ũ������������Һ�ĵ����Ա�b�㻹ǿ����a��b��c���ˮ��Һ������������ǿ,��ȷ��C����δ�μ�NaOH��Һʱ����Һ��pH="2," c(H+)=10-2mol/L��NaOH��ǿ���ȫ���룬��NaOH��Һ����20mlʱ��ǡ������HA��ȫ��Ӧ����ʱ��Һ��pH>7��˵���õ�����ǿ��ǿ�����Σ����HA�����ᣬ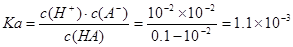 ������D��a��ʱ�������c(H+)=10-3mol/L�� c��ʱ�������c(H+)=10-11mol/L��c(OH-)=Kw��c(H+)=10-14��10-11=10-3mol/L�����Զ��߶�ˮ�ĵ���ƽ�������������ͬ�������������ʾ��Һ��H2O�ĵ���̶���ͬ����ȷ��
������D��a��ʱ�������c(H+)=10-3mol/L�� c��ʱ�������c(H+)=10-11mol/L��c(OH-)=Kw��c(H+)=10-14��10-11=10-3mol/L�����Զ��߶�ˮ�ĵ���ƽ�������������ͬ�������������ʾ��Һ��H2O�ĵ���̶���ͬ����ȷ��
���㣺��������ǿ�����жϡ�����Ũ�ȵļ��㼰��ˮ����ƽ����ƶ���Ӱ���֪ʶ��
�����Ѷȣ�����
3������� ��ʵ��ࣩ��13�֣������£�ȡ0.2 mol��L��1 HCl��Һ��0.2 mol��L��1 MOH��Һ�������ϣ����Ի�Ϻ���Һ����ı仯������û����Һ��pH��6���Իش��������⣺
��1�������Һ����ˮ�������c (H+) 0.2 mol��L��1 HCl��Һ����ˮ�������c (H+) (�>��<��=��)��
��2������������������ʽ�ľ�ȷ����������������֣���
c (Cl��) ?c (M+)�� mol��L��1��c (H+) ?c (MOH) �� mol��L��1��
��3����������ȡ0.2 mol��L��1 MOH��Һ��0.1 mol��L��1 HCl��Һ�������ϣ���û����Һ��pH��7��˵��MOH�ĵ���̶� (�>��<��=��)MCl��ˮ��̶ȡ���Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
��4����������pH��3��������pH��11�İ�ˮ��Һ�������ϣ�������Һ��pH��7���>��<��=������
�ο��𰸣�17.(ʵ���) ��1�� > ��2��9.9��
���������
�����������1���������Ũ�ȵ������MOHǡ�÷�Ӧ�����Σ��õ�������Һ�����ԣ�˵��������ǿ�������Σ������������ӵ��δٽ�ˮ���룬������ˮ���룬���Ի����Һ��ˮ�������c��H+����0.2 mol?L-1 HCl��Һ��ˮ�������c��H+������2�����ݵ���غ��c��Cl-��-c��M+��=c��H+��-c��OH-��=10-6 mol/L-10-8 mol/L=9.9��10-7mol?L-1�����������غ�� c��H+��-c��MOH��=c��OH-��=1.0��10-8mol?L-1����3�����������ȡ0.2mol?L-1 MOH��Һ��0.1mol?L-1 HCl��Һ�������ϣ���Һ�е�������MCl��MOH����û����Һ��pH��7��˵����ĵ���̶�С���ε�ˮ��̶ȣ���Һ�����ԣ���c��H+����c��OH-������ϵ���غ�֪c��Cl-����c��M+����������������Ũ�ȴ��������Ӻ�����������Ũ�ȣ�������Һ�и�����Ũ���ɴ�С��˳��Ϊc��Cl-����c��M+����c��H+����c��OH-������4����������pH=3��������pH=11�İ�ˮ��Һ�������ϣ���ˮ��Ũ�ȴ���0.001mol/L���������Ũ��Ϊ0.001mol/L���������Ϻ�ˮ��������Һ��ʾ���ԣ���Һ��pH��7��
���㣺���������ʱ�Ķ����жϺ��й�PHֵ�ļ��㡣
�����Ѷȣ�����
4��ѡ���� ���е��뷽��ʽ�������
A.NaHCO3=Na++H++CO32-
B.NaHSO4=Na++H++SO42-
C.Al2O32Al3++3O2-
D.CaCO3=Ca2++CO32-
�ο��𰸣�A
���������������ǿ����ʵĵ����á��T������ѭ�����غ㶨�ɺ͵���غ㣬��ע��ԭ���Ų��ɲ�֣��Դ������
���A��NaHCO3Ϊǿ����ʣ����뷽��ʽΪNaHCO3=Na++HCO3-����A����
B��NaHSO4Ϊǿ����ʣ����뷽��ʽΪNaHSO4=Na++H++SO42-����B��ȷ��
C��Al2O3Ϊǿ����ʣ����뷽��ʽΪAl2O3 2Al3++3O2-����C��ȷ��
2Al3++3O2-����C��ȷ��
D��CaCO3Ϊǿ����ʣ����뷽��ʽΪCaCO3=Ca2++CO32-����D��ȷ��
��ѡA��
���������⿼����뷽��ʽ����д����ȷ����ʵ�ǿ�������뷽��ʽ��ѭ����غ㼰�����غ㶨�ɼ��ɽ���״���Ϊѧ�����������е�ԭ���ţ�ע��A��B�ıȽϣ�
�����Ѷȣ���
5��ѡ���� ���и�����Һ������pH��ͬʱ�����ʵ���Ũ��������
A��KOH
B��NH3��H2O
C��Ba(OH)2
D��NaOH
�ο��𰸣�B
�����������
�����Ѷȣ�һ��