微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)8 g CH4的物质的量为 ,在标准状况下所占的体积约为 ;
(2)100mL 1 mol・L-1Al2(SO4)3溶液中含Al3+离子 mol,含SO42-离子 个。
(3)0.6mol O2与0.4mol O3质量之比为 ,分子个数之比为 ,原子个数之比 ,它们在同温同压下的体积比是 。
参考答案:(每空2分,共8分)(1)0.5mol;11.2L (2)0
本题解析:
试题分析:(1)甲烷的摩尔质量是16g/mol,则根据n=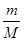 可知,8 g CH4的物质的量=8g÷16g/mol=0.5mol;标准状况下气体的摩尔体积是22.4L/mol,则根据n=
可知,8 g CH4的物质的量=8g÷16g/mol=0.5mol;标准状况下气体的摩尔体积是22.4L/mol,则根据n=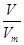 可知,在标准状况下所占的体积约为0.5mol×22.4L/mol=11.2L。
可知,在标准状况下所占的体积约为0.5mol×22.4L/mol=11.2L。
(2)100mL 1 mol・L-1Al2(SO4)3溶液中硫酸铝的物质的量=0.1L×1mol/L=0.1mol,则根据Al2(SO4)3=2Al3++3SO42-可知,溶液中含Al3+离子的物质的量=0.1mol×2=0.2mol。溶液中含SO42-离子的物质的量=0.1mol×3=0.3mol,则个数=0.3mol×6.02X1023/mol=1.806X1023个。
(3)氧气和臭氧的相对分子质量分别是32和48,则根据n=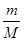 可知,0.6mol O2与0.4mol O3质量之比为0.6mol×32g/mol:0.4mol×48g/mol=1:1;根据N=nNA可知,分子个数之比为0.6mol:0.4mol=3:2;原子个数之比=0.6mol×2:0.4mol×3=1:1;根据n=
可知,0.6mol O2与0.4mol O3质量之比为0.6mol×32g/mol:0.4mol×48g/mol=1:1;根据N=nNA可知,分子个数之比为0.6mol:0.4mol=3:2;原子个数之比=0.6mol×2:0.4mol×3=1:1;根据n=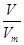 可知,它们在同温同压下的体积比=0.6mol:0.4mol= 3:2。
可知,它们在同温同压下的体积比=0.6mol:0.4mol= 3:2。
考点:考查物质的量、微粒数、气体体积以及物质的量浓度的有关计算
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温下,0.05 mol・L-1 Fe2(SO4)3溶液中含Fe3+数目为0.1NA
B.标准状况下,22.4 L甲苯中含C-H数目为8 NA
C.常温下,9.2 g NO2和N2O4的混合气体中含有的氮原子数目为0.2 NA
D.1 mol氯气和足量NaOH溶液反应转移的电子数目为2NA
参考答案:C
本题解析:
试题分析:A.只知道浓度缺少溶液的体积,所以无法确定溶液中微粒的数目的多少,错误;B.标准状况下,甲苯的状态是液态,不能使用气体摩尔体积,错误;C.常温下,9.2 g NO2和N2O4的混合气体中含有的氮原子数目为0.2 NA,正确;D.1 mol氯气和足量NaOH溶液反应转移的电子数目为NA,错误。
考点:考查阿伏加德罗常数的有关计算的知识。
本题难度:一般
3、选择题 在下列溶液中Cl-物质的量浓度最大的是( )
A.0.5L0.1mol/L的NaCl溶液
B.100mL0.2mol/L的MgCl2溶液
C.50mL0.2mol/L的AlCl3溶液
D.1L1mol/L的盐酸溶液
参考答案:A、0.5L0.1mol/L的NaCl溶液中氯离子的物质的量
本题解析:
本题难度:简单
4、填空题 标准状况下,甲烷和一氧化碳的混合气体共8.96L,其质量为7.6g,则混合气体中甲烷的体积为 ,一氧化碳的质量为 。
参考答案:6.72 L、 2.8
本题解析:
试题分析:混合气体的物质的量为 =0.4mol,假设甲烷和一氧化碳的物质的量分别为x和y,则x+y=0.4mol,16x+28y=7.6g,解得x=0.3mol,y=0.1mol,故甲烷的体积为0.3molx22.4L/mol=6.72L,一氧化碳的质量为0.1molx28g/mol=2.8g,答案为6.72L;2.8g
=0.4mol,假设甲烷和一氧化碳的物质的量分别为x和y,则x+y=0.4mol,16x+28y=7.6g,解得x=0.3mol,y=0.1mol,故甲烷的体积为0.3molx22.4L/mol=6.72L,一氧化碳的质量为0.1molx28g/mol=2.8g,答案为6.72L;2.8g
考点:物质的量的有关计算
本题难度:一般
5、计算题 常温下,在28.9g水中溶解12.1g Cu(NO3)2・3H2O,恰好达到饱和,设该溶液密度为1.20g /cm3,求:
(1)该溶液中Cu(NO3)2的物质的量和溶液的体积
(2)该溶液中Cu(NO3)2的物质的量浓度
(3)取出20.0ml该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
参考答案:(1)n=0.05mol;V溶液=34.167ml
本题解析:
本题难度:一般