��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��ͬ������ͬŨ�ȵ�NaCN��NaF��ϡ��Һ��ǰ�ߵ�pHֵ���ں��ߣ���ͬ�����±Ƚ�ͬŨ��ͬ���������Һ�еĹ�ϵ��������ȷ����
A��c(CN-)>c(F-)
B��c(Na+)��c(CN-)��c(F-)
C��NaCNˮ��̶ȱ�NaF��
D����������ˮ�����������
�ο��𰸣�C
���������
���������NaCN��pHֵ����NaF��CN-ˮ��̶ȴ���F-������c(CN-)<c(F-)����A����c(Na+)> c(F-)> c(CN-)����B���� NaCNˮ��̶ȱ�NaF��C��ȷ����������ˮ������������ȣ���D����
���㣺���⿼���ε�ˮ�⡣
�����Ѷȣ�һ��
2��ʵ���� ��1��ij��ȤС����ʵ����̽����ҵ�ϳ�����Ļ�ѧԭ����
�ٰ��Ĵ�������ͼa��̽�����Ĵ������ļ���װ�ã�ʵ���й۲쵽��ƿ�в�˿���ֺ��ȣ��к���ɫ�������ɻ���̲��������̵ijɷ��� ���ѧʽ����
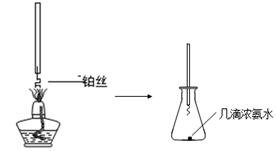

ͼa ͼb
��NO2�����գ���ͼb��ʾ����һƿNO2������ˮ���У���ˮ���ƿ�����Ƭ���ɹ۲쵽�������� ��
��2������������Һ��Fe3+ˮ������ػ�ɫ������Fe(NO3)3��ҺΪ�������ʵ��̽��Ӱ������ˮ��̶ȵ����ء�
��д��Fe(NO3)3ˮ������ӷ���ʽ ��
�ڲ���ʾ������±�ʵ�鷽������ơ�
��ѡ���ϣ�0.05mol?L-1Fe(NO3)3��0.5mol?L-1Fe(NO3)3��1.0mol?L-1HNO3��1.0mol?L-1NaOH��NaHCO3���塢����ˮ����ˮ����pH�Ƽ���������������
����Ӱ������
| ʵ�����
| Ԥ������ͽ���
|
��Һ�������
| ȡ����0.5mol?L-1Fe(NO3)3���Թ��У����뼸��1mol?L-1HNO3��
| �ػ�ɫ��Һ��ɫ��dz��˵����Һ������ǿ������Fe(NO3)3��ˮ�⡣
|
�ε�Ũ��
|
|
|
|
|
�ο��𰸣���1������4�֣��� NH4NO3 &#
���������
�����������1���ٰ�����������������������NO��ˮ��NO������е�������Ӧ���ɺ���ɫ�����������������������ˮ��Ӧ�����������ɣ������백����Ӧ���ɰ�ɫ��������泥�����̵ijɷ���NH4NO3��
�ڶ�����������ˮ�������������ɫ����NO��ͬʱƿ��ѹǿ��С�����Կ�������ƿ�ں���ɫ������ʧ������ƿ�е�Һ����������
��2����Fe(NO3)3ˮ�������������������ᣬ���ӷ���ʽΪFe3+ + 3H2O  Fe(OH)3 + 3H+ Fe(OH)3 + 3H+
��Ӱ����ˮ��̶ȵ�������Ũ�ȡ��¶ȡ�����������ˮ������ӷ���ʽ�ж�����������Ũ��ƽ�������ƶ����ɲ��ò�ͬŨ�ȵ�Fe(NO3)3��Һ������ʵ�飬�ⶨ��Һ��pH���ж�ˮ��̶ȵĴ�С������H+ Ũ��ƽ�������ƶ�����Һ�ػ�ɫ��dz��ˮ�ⷴӦ�ɿ������кͷ�Ӧ���淴Ӧ�����������ȷ�Ӧ�������¶�ƽ�⣬�����ƶ�����Һ�ػ�ɫ�������ʵ�����±���
Ӱ������
ʵ�����
Ԥ������ͽ���
���ε�Ũ��
����Ͳȡ10mL Fe(NO3)3���ձ��У���pH�Ʋ��pHֵ����ȡ90mL����ˮ�����ձ�����ֽ��裬����pH�Ʋ��pHֵ��
ǰ����pHֵ֮��С��1��˵����ˮϡ�ͺ�ƽ�����ƣ����ɸ����H+��������Fe(NO3)3Ũ�ȣ�����Fe(NO3)3ˮ�⡣
����ε�Ũ��
��pH�Ʒֱ�ⶨ0.05mol?L-1Fe(NO3)3��0.5mol?L-1Fe(NO3)3��pH�����Ƚϴ�С��
������Һ��pHֵ֮��С��1��˵������c(Fe(NO3)3)������Fe(NO3)3ˮ�⡣
����ε�Ũ��
ȡ����0.5mol?L-1Fe(NO3)3���Թ��м�������NaHCO3���塣
��Һ��ɫ���˵����������NaHCO3����ɼ���c(H+)�ٽ�Fe(NO3)3ˮ�⡣
����ε�Ũ��
ȡ����0.5mol?L-1Fe(NO3)3���Թ��м��뼸��1.0mol?L-1NaOH
��������ɫ�������ػ�ɫ��Һ�����ɫ��˵������NaOH�ɼ���c(H+)�ܴٽ�Fe(NO3)3ˮ�⡣
�������¶�
ȡ����0.5mol?L-1Fe(NO3)3���Թ��У����þƾ��Ƽ���һ��ʱ�䣬�۲���Һ��ɫ
���Ⱥ���Һ��ɫ���˵�������¶ȴٽ�Fe(NO3)3ˮ�⡣
��۽����¶�
ȡ����0.5mol?L-1Fe(NO3)3���Թ��У��ٽ��Թ����ڷ��б�ˮ�������ձ���һ��ʱ�䣬�۲���Һ��ɫ
�ػ�ɫ��Һ��ɫ��dz��˵�������¶�������Fe(NO3)3ˮ�⡣
���㣺���鰱���Ĵ��������������������գ������ӵ�ˮ�⼰Ӱ��ˮ��̶ȵ�������ʵ�����
�����Ѷȣ�����
3��ѡ���� ��ϡ������Һ�����백ˮ������Һ��c(NH4��)=2c(SO42��)ʱ����Һ��pH �� ��
A������7
B������7
C����7
D�����ж�
�ο��𰸣�A
������������ݵ���غ��֪��2c(SO42��)+c(OH��)��c(NH4��)��c(H��)�����������Һ��c(NH4��)=2c(SO42��)ʱ��c(OH��)��c(H��)������Һ�����ԣ���ѡA��
�����Ѷȣ�һ��
4��ѡ���� ��һ�������·������з�Ӧ��������������ˮ�ⷴӦ���ǣ� ? �� A��NH4++2H2O?NH3?H2O+H3O+
B��HCO3-+H2O?H3O++CO32-
C��HS-+H+�TH2S
D��Cl2+H2O?H++Cl-+HClO
�ο��𰸣�A
���������
�����Ѷȣ���
5��ѡ���� Ϊ������NH4+��Ũ����Cl����Ũ�ȱ�Ϊ1��1����Һ������NH4Cl��Һ�м�������( )��Ũ���� ��NaCl���� ��Ũ��ˮ ��NaOH����
A����
B����
C���٢�
D���ۢ�
�ο��𰸣�A
���������NH4Cl��Һ��NH4+Ҫ����ˮ�⣬ʹ��Һ�����ԣ�����Һ��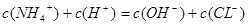 ����NH4+��Ũ����Cl����Ũ�ȱ�Ϊ1��1������Һ�� ����NH4+��Ũ����Cl����Ũ�ȱ�Ϊ1��1������Һ��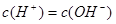 ��Ϊ������Һ��Ϊ�����������������ӣ�Ӧ����Ũ��ˮ��������ȷѡ��ΪA�� ��Ϊ������Һ��Ϊ�����������������ӣ�Ӧ����Ũ��ˮ��������ȷѡ��ΪA��
�����Ѷȣ�һ��
|