微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到实验目的是
A.将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl固体
D.将表面有铜绿[Cu2(OH)2C03]的铜器放入盐酸中浸泡,除去铜绿
参考答案:D
本题解析:分析:A.反应后的混合物与水混合的顺序错误;
B.常温下铜与氯气不反应;
C.氯化铜溶液加热促进水解;
D.Cu2(OH)2C03能溶于盐酸.
解答:A.铜丝与浓硫酸加热生成硫酸铜后,再把混合物加入水中形成硫酸铜溶液,而不能把水加入反应混合物中,防止剩余的浓硫酸稀释时溅出,所以故A错误;
B.常温下铜与氯气不反应,因此观察不到现象,故B错误;
C.氯化铜溶液加热促进水解,水解生成的HCl受热挥发,最后氯化铜完全水解得到Cu(OH)2,故C错误;
D.Cu2(OH)2C03能溶于盐酸,所以能用盐酸出去铜绿,故D正确;
故选D.
点评:本题考查了铜及其化合物的性质,以及盐类的水解,题目难度不大.
本题难度:简单
2、选择题 用铝箔包着2.3g金属钠,放入50ml水中,放出的H2体积(标准状况)是( )
A.等于2.24L
B.等于1.12L
C.大于1.12L
D.小于1.12L
参考答案:C
本题解析:由2Na+2H2O=2NaOH+H2↑知2.3g金属钠反应生成H2体积(标准状况)是1.12L,但铝箔与生成的NaOH还可以继续反应:2Al+2NaOH+2H2O=2NaAlO2+3 H2↑,所以放出H2体积(标准状况)大于1.12L,答案选C。
本题难度:简单
3、选择题 准确称取6.0g铝土矿样品(含SiO2、Fe2O3),加入100mL稀硫酸中,充分反应后向滤液中加入10mol?L-1NaOH溶液,产生沉淀的质量/g(纵坐标)和加入NaOH溶液体积/mL(横坐标)之间的关系如下图所示。则所用硫酸物质的量浓度为(mol?L-1)
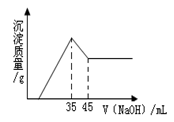
A.1.75
B.3.50
C.0.85
D.无法确定
参考答案:A
本题解析:略
本题难度:简单
4、填空题 哥伦比亚号航天飞机曾用金属铝粉和高氯酸铵混合物作为固体燃料。加热铝粉使其氧化并放出大量热量,促使混合物中另一种燃料分解。m摩尔高氯酸铵分解时除产生2m摩尔水蒸气和m摩尔氧气外,其他组成元素均以单质形式放出,因而产生巨大的推动力。试写出其中涉及的化学方程式:
(1)________________________________________________________________。
(2)________________________________________________________________。
根据此反应原理,1摩尔高氯酸铵分解所产生的气体有_______________摩尔。
参考答案:(1)4Al+3O2 本题解析:铝粉燃烧反应是同学们熟悉的反应,它不是本题的难点,高氯酸铵的分解才是本题的关键。高氯酸铵分解,反应物就是本身,产物已知有水蒸气和氧气,根据元素守恒,产物中还缺少氮元素和氯元素,根据已知信息,它们是氮气和氯气。高氯酸铵的配平,可首先暂定高氯酸铵、水蒸气和氧气的化学计量数为1、2、1,再根据氧化还原守恒规律或氮、氯原子守恒来配平氮气和氯气的化学计量数,最后同时扩大2倍即得答案。
本题解析:铝粉燃烧反应是同学们熟悉的反应,它不是本题的难点,高氯酸铵的分解才是本题的关键。高氯酸铵分解,反应物就是本身,产物已知有水蒸气和氧气,根据元素守恒,产物中还缺少氮元素和氯元素,根据已知信息,它们是氮气和氯气。高氯酸铵的配平,可首先暂定高氯酸铵、水蒸气和氧气的化学计量数为1、2、1,再根据氧化还原守恒规律或氮、氯原子守恒来配平氮气和氯气的化学计量数,最后同时扩大2倍即得答案。
本题难度:简单
5、选择题 铝元素在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一而加以控制.铝及其化合物在下列场合使用时都须加以控制的是( )
①制电线、电缆
②制包糖果用的铝箔
③用明矾净水
④制炊具
⑤用明矾和苏打作食物膨化剂
⑥用氢氧化铝制胃药
⑦制防锈油漆.
A.①②④⑤⑥⑦
B.③④⑤⑥
C.②③④⑤⑥
D.③④⑤⑥⑦
参考答案:铝是食品污染源之一,所以只要与人口腔接触的含有铝的物质就需要
本题解析:
本题难度:简单