微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 钛(Ti)因为具有神奇的性能越来越引起人们的关注,常温下钛不和非金属、强酸反应,红热时,却可与常见的非金属单质反应,钛是航空、军事、电力等方面的必需原料。地壳中含钛铁矿石之一是金红石(TiO2),目前大规模生产钛的方法是:
第一步:金红石、炭粉混合,在高温条件下,通入Cl2制得TiCl4和一种可燃气体,该反应的化学方程式为__________________________________________________________,该反应的还原剂是__________。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)写出此反应的化学方程式____________________________________________________。
(2)简述从上述所得产物中获得金属钛的步骤。
__________________________________________________________________。
参考答案:第一步:TiO2+2C+2Cl2 本题解析:(1)第一步反应的反应物有TiO2、Cl2和C,产物有TiCl4和另一种可燃气体,从元素守恒来看,可燃气体中只能有C和O,那么它是CO还是CO2呢?在高温条件下,CO2的稳定性不如CO,即在高温条件下应为CO。第二步反应是置换反应,比较容易给出方程式。
本题解析:(1)第一步反应的反应物有TiO2、Cl2和C,产物有TiCl4和另一种可燃气体,从元素守恒来看,可燃气体中只能有C和O,那么它是CO还是CO2呢?在高温条件下,CO2的稳定性不如CO,即在高温条件下应为CO。第二步反应是置换反应,比较容易给出方程式。
(2)反应中可能用到过量的金属镁,因钛不溶于强酸,所以可以用强酸将镁与钛分离开。
本题难度:简单
2、选择题 下列描述的物质一定是金属单质的是???????????????????????????????????
A.能失去电子的物质
B.能得到电子的物质
C.由含11个质子的原子构成的物质
D.能与水反应的物质
参考答案:C
本题解析:
试题分析:A.能失去电子的物质是还原剂,如Fe2+,不是金属单质;B.能得到电子的物质一定不是金属单质,金属单质只能失去电子; C.由含11个质子的原子构成的物质是金属Na,正确;D.能与水反应的物质有Na2O等,不是金属单质。
本题难度:一般
3、填空题 (10分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。写出此反应的化学方程式?????????????????。
(2)上述反应中的氧化剂是?????????????,氧化产物是??? ??????????。
??????????。
(3) As2S3和HNO3有如下反应:As2S3+ 10HNO3=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成1mol H3AsO4,则反应中转移电子的物质的量为???????。
(4)在3Cu + 8HNO3= 3Cu(NO3)2 + 2NO↑+4H2O的反应中,有6.4g铜被氧化,参加反应的HNO3的质量是____________g,被还原的HNO3的质量是__________g。
(5)在一定条件下,P bO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1mol C
bO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1mol C r2O72-
r2O72-
反应所需PbO2的物质的量为__________ ____。
____。
参考答案:(1)2As2S3+2SnCl2 本题解析:略
本题解析:略
本题难度:一般
4、选择题 实验室常用浓盐酸和二氧化锰反应来制取少量氯气,反应的化学方程式为:
MnO2 + 4HCl(浓) MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。
取8.7g的MnO2与50mL足量的浓盐酸发生反应制取氯气。求:
(1)生成的还原产物的物质的量是多少?
(2)(忽略Cl2的溶解)产生的氯气在标准状况下的体积为多少?
(3)反应中被氧化的HCl的物质的量是多少?
参考答案:(1)0.1mol?????? (2 )? 2.24L???
本题解析:
试题分析:(1)二氧化锰的摩尔质量是87g/mol
则根据 n=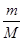 可知,8.7二氧化锰的物质的量=8.7g÷87g/mol=0.1mol
可知,8.7二氧化锰的物质的量=8.7g÷87g/mol=0.1mol
根据方程式可知,二氧化锰是氧化剂,其还原产物是MnCl2
则根据原子守恒可知,还原产物氯化锰的物质的量是0.1mol
(2)根据方程式可知
本题难度:一般
5、填空题 (14分)Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
第一电离能
| 离子半径
| 熔点
| 酸性
|
Si S
| O2- Na+
| NaCl Si
| H2SO4 HClO4
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
参考答案:
(1)第三周期,第ⅠA族 2
本题解析:
试题分析:(1)S的最外层有6个电子,为3s23p4,3p能级三个轨道、四个电子,依据泡利原理和洪特规则,先每个轨道排1个,方向相同,排满后再排,方向相反,故有两个孤对电子;硅,核电核数为14,根据构造原理可以排出。
(2)第一电离能同周期从左往右逐渐增大趋势,但有几个反常,故有Si<S;具有相同的电子层结构,核电荷越多半径越小,故有O2-<Na+;一般熔沸点原子晶体大于离子晶体;同周期从左到右非金属性逐渐增强,非金属性越强其最高价氧化物对应水化物的酸性越强。
(3)该反应为氧化还原反应,Cu从+1到+2价,O2做氧化剂,从0价到-2价。
(4)氯气做氧化剂从0价到-1价,亚氯酸根从+3到+4价。
考点:物质结构、元素及化合物性质、氧化还原反应、热化学反应方程式等
本题难度:一般
|