��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��Fe��Cu�Ļ�Ϸ�ĩ���뵽100 mL 4 mol/Lϡ�����г�ַ�Ӧ��
(1)����Ӧ����Cuʣ�࣬�����Һ��һ���е���������???????�������е���������???????????????????��
(2)����Ӧ�����Һ����Fe3��������Һ��һ�����е���������???????�����ܺ��е���������?????????????????????????????????????????????????????????��
(3)�����Ӧ�����Һ������ʣ�࣬�����Ľ����������Ϊ?????????????????????????��
(4)��������Fe��Cu��������Ϊ7��8����ʹHNO3��ȫ��Ӧ�Ľ�����С����Ϊ????????????????????????????????????????????????????????????????????��
�ο��𰸣�(1)Fe2����Cu2��
(2)Cu2����Fe2����H
���������������Ҫע�����ϡHNO3������ͭ����ʱ�ķ�Ӧ˳����Fe��Ӧ����Fe3��������Cu��Ӧ����Cu2������Fe3����Fe��Ӧ����Fe2����(1)����Ӧ����Cuʣ�࣬�����Һ��һ���е���������Fe2���������е���������Cu2����(2)����Ӧ����Fe3���������Һ��һ���е���������Cu2���������е���������Fe2����H�����������߲���ͬʱ�������ڣ�(3)���������������̿�֪��ֻ������ͭ�ķ�Ӧʱ����Ľ������������ģ���3Cu��8HNO3�ɽ����Cu���������Ϊ9.6 g��(4)��Ҫ���������Ҫ��С�����Լ����
�����Ѷȣ�һ��
2��ѡ����&n bsp; �����£���ij200 mL��ϡ�����ϡ����Ļ����Һ�������ؼ������ۣ�������������������������ӵı仯��ͼ��ʾ����������ֻ����ԭΪNO����, Fe�����ԭ������Ϊ56���������йط����������
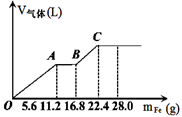
A��ԭ�������NO3�������ʵ���Ϊ0.2 mol
B��ԭ�������H2SO4���ʵ���Ũ��Ϊ2mol/L
C��OA����BC�η�Ӧ�е���ת�Ƶ����ʵ���֮��Ϊ2:1
D��ȡ20mLԭ������ˮϡ����1L����Һ��pH��1
�ο��𰸣�C
���������
����������������������ᣬ�������������Ӧ����OA�α�ʾ�������ᷴӦ������������NO��ˮ�����ӷ���ʽΪFe��4H����NO3��=Fe3����2H2O��NO������NO3����ȫ����ԭ������������ۣ������ӿ�ʼ�������ۣ���AB�ε����ӷ���ʽΪFe��2Fe3��=3Fe2�����������������������������û���Ӧ������������BC�η�Ӧ�����ӷ���ʽΪFe��2H��=F2��H2�����ݴ˿����жϡ�A����Aʱ��Һ�е�NO3��β������ԭΪNO����ʱ��������������11.2g�����ʵ�����11.2g��56g/mol��0.2mol����
�����Ѷȣ�һ��
3������� д����ʽ��
��1��______H2O2+______KMnO4+______H2SO4�T______MnSO4+______O2+______K2SO4+______H2O
��2����д�������û���Ӧ��Ҫ��a���ǽ�������֮����û�����b���ڷ���ʽ�����ַǽ������ʱ����Dz�ͬ����ģ�______��______��
�ο��𰸣���1����Ӧ�����ʵĻ��ϼ۱仯��KMnO4��MnSO4��MnԪ
���������
�����Ѷȣ�һ��
4������� ��4�֣���ɲ���ƽ���л�ѧ����ʽ��FeO + ��HNO3������Fe(NO3)3 + NO��+ ��???��
�÷�Ӧ����������????????��������2mol NOʱ��ת�Ƶĵ�����Ϊ????????NA��
�ο��𰸣�
 �����������
�����������
�����Ѷȣ�һ��
5��ѡ���� ��ˮ�ȷ��Ʊ�Fe3O4���������ܷ�Ӧ���£�
3Fe2��+ 2S2O32��+O2+4OH��= Fe3O4 + S4O62��+2H2O������˵����ȷ���ǣ�???��
A���ڷ�Ӧ��1molO2������3mol Fe2��
B����ԭ����Fe2������������S2O32����O2
C��ÿ����1mol Fe3O4��ת��3mol����
D����ת��1mol����ʱ������56gS2O32��
�ο��𰸣�D
�������������������ԭ��Ӧ���֪ʶ��
��Ӧ�������������ӵĻ��ϼ���+2������+3�ۣ�Fe3O4��������+3�������� S2O32���е��ĸ���ȫ��ת��ΪS4O62�������廯�ϼ���+8������+10�ۣ�����2�ۣ��������ļۣ�����������Ԫ����0�۽�����2�ۣ������ļۣ���Ӧ�����ĸ����ӵ�ת��
���Ի�ԭ��ΪFe2����2S2O32����������ΪO2
A��1molO2�����ˣ�mol Fe2��
B����ԭ��ΪFe2����2S2O32����������ΪO2
C��ÿ����1mol Fe3O4����ת�ƣ�mol����
D��
�����Ѷȣ�һ��