微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 恒容密闭容器中进行的可逆反应2NO2?2NO+O2,达到平衡状态的是( )
①单位时间内生成a?mol O2的同时生成2a?mol?NO2
②单位时间内生成a?mol?O2的同时生成2a?mol NO
③混合气体的颜色不再改变
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态.
A.①③⑤
B.②④⑤
C.①③④
D.①②③④⑤
参考答案:此题列出了判断可逆反应是否达到平衡状态的各种可能情况,应从平
本题解析:
本题难度:一般
2、选择题 下列说法中可以说明2HI(g) H2(g)+I2(g)已达到平衡状态的是(???)
H2(g)+I2(g)已达到平衡状态的是(???)
(1)单位时间内生成n mol H2的同时生成n mol HI
(2)一个H―H键断裂的同时有两个H―I键断裂
(3)c(HI)= c(I2)
(4)反应速率υ(H2)=υ(I2)=0.5υ(HI)
(5)c(H2)∶c(I2)∶c(HI)=2∶1∶1
(6)温度和体积一定时,某一生成物浓度不再变化
(7)温度和体积一定时,容器内压强不再变化
(8)条件一定,混合气体的平均相对分子质量不再变化
(9)温度和体积一定时,混合气体的颜色不再发生变化
(10)温度和压强一定时,混合气体的密度不再发生变化
参考答案:(2)(6)(9)
本题解析:判断可逆反应是否已达平衡状态,关键是紧紧围绕这着“等”[υ(正)=υ(逆)]与“定”(条件一定,反应混合物的含量保持不变)这两个因素来判断。而“定”并非是指反应混合物的含量“相等”或者“成比例”。特别反应2HI H2+I2(g)的气体的计量数前后不变。(1)虽然表示的是不同的反应方向,但不能证明υ(正)=υ(逆)
H2+I2(g)的气体的计量数前后不变。(1)虽然表示的是不同的反应方向,但不能证明υ(正)=υ(逆)
本题难度:一般
3、选择题 将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:
2SO2(g)+O2(g)?
催化剂
△
?2SO3(g)(正反应放热).判断该反应达到平衡状态的标志是( )
A.SO2和SO3浓度相等
B.SO2百分含量保持不变
C.容器中气体的压强不变
D.SO3的生成速率与SO2的消耗速率相等
参考答案:A、可逆反应到达平衡时SO2和SO3浓度不一定相等,与二氧化
本题解析:
本题难度:一般
4、实验题 (7分)下表数据是在某高温下,金属镁和镍分别在氧气中进行氧化反应时,在金属表面生成氧化薄膜的实验记录。
反应时间t/h
| 1
| 4
| 9
| 16
| 25
|
MgO层厚y/nm
| 0.05a
| 0.20a
| 0.45a
| 0.18a
| 1.25a
|
NiO层厚y′/nm
| B
| 2b
| 3b
| 4b
| 5b
注:a和b均为与温度有关的常数。
(1)金属高温氧化腐蚀速率可以用金属氧化膜的生长速率来表示,其理由是_______________
_______________________________________________________________________________;
(2)金属氧化膜厚y跟时间t所呈现的关系是(填“直线”、“抛物线”、“对数”或“双曲线”等类型):MgO氧化膜的膜厚y与时间t的关系属________型;NiC氧化膜的膜厚y′与时间t的关系属________型;
(3)Mg与Ni比较,哪一种金属具有更良好的耐氧化腐蚀性?阐述其理由。
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
_______________________________________________________________________________。
参考答案:(1)反应速率可用反应物的消耗速率表示,也可用产物的生成速率
本题解析:由表中所列数据及题干中的提示(直线、抛物线、对数或双曲线等类型)不难导出以下关系式:y=0.05at;y′=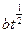 ,由此可得出结论:MgO膜厚y与时间t的关系为直线型;NiO膜厚y′与时间t的关系为抛物线型。由以上所得两个关系式可知,y′随时间t增长要比y随时间t增长得慢,所以镍的耐高温腐蚀性要比镁的好。 ,由此可得出结论:MgO膜厚y与时间t的关系为直线型;NiO膜厚y′与时间t的关系为抛物线型。由以上所得两个关系式可知,y′随时间t增长要比y随时间t增长得慢,所以镍的耐高温腐蚀性要比镁的好。
本题难度:简单
5、选择题 已知反应3A(g)+B(g)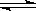 C(s)+4D(g)+Q,右图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是:①增大B的浓度?②升高反应温度?③缩小反应容器的体积(加压)?④加入催化剂(???? ) C(s)+4D(g)+Q,右图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是:①增大B的浓度?②升高反应温度?③缩小反应容器的体积(加压)?④加入催化剂(???? )

A.①②
B.①③
C.②③
D.③④
参考答案:D
本题解析:
试题分析:根据图像可知,使反应过程按b曲线进行,和a曲线比较,反应的平衡状态没有变化,但反应速率加快,达到平衡的时间减少。由于该反应是反应前后体积不变的可逆反应,因此改变的条件只可能是使用了催化剂或增大压强,答案选D。
点评:外界条件对平衡状态的影响一般是温度、浓度、压强等,在具体判断时一般遵循勒夏特列原理进行分析
本题难度:一般
|