��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
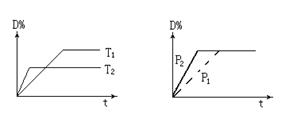
1��ѡ���� ���淴ӦmA(g)+nB(s) rC(g)+qD(g)�ڷ�Ӧ�����У������������䣬D������ٷֺ������¶�T��ѹǿP��ϵ��ͼ��ʾ��������������ȷ����
rC(g)+qD(g)�ڷ�Ӧ�����У������������䣬D������ٷֺ������¶�T��ѹǿP��ϵ��ͼ��ʾ��������������ȷ����
A����ѧ����ʽϵ��m+n=r��q
B��ʹ�ô�����D�����ʵ�����������
C���¶Ƚ��ͣ���ѧƽ��������Ӧ�����ƶ�
D������B�Ŀ���ԽС����ӦԽ�죬������ƽ��������Ӧ�����ƶ�
�ο��𰸣�C
���������
���������A������ͼ��֪��ѹǿΪP2�ȵ���ƽ�⣬��P2��P1������ѹǿ��D%���䣬��ƽ�ⲻ�ƶ�����Ӧ��BΪ���壬��m=r+q����A����B��ʹ�ô��������̵���ƽ��ʱ�䣬ƽ�ⲻ�ƶ���D%�IJ��䣬��B����C������ͼ֪���¶�T2Ϊ�ȵ���ƽ�⣬��T2��T1�������¶ȣ�D%��С����ƽ�����淴Ӧ�ƶ�������¶Ƚ��ͣ���ѧƽ��������Ӧ�����ƶ���C��ȷ��D��BΪ���壬����B�Ŀ���ԽС���Ӵ����Խ��ӦԽ�죬����ƽ���ƶ�û��Ӱ�죬��D����ѡC��
���㣺���黯ѧƽ����ƶ�����ѧƽ��Ӱ�����ء���ѧƽ��ͼ���
�����Ѷȣ�һ��
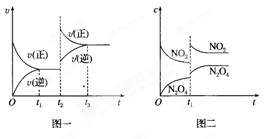
2��ѡ���� ��֪ͼһ��ʾ���ǿ��淴ӦC0(g)+H2(g)  C(s)+H20(g)?��H>O��ѧ��Ӧ����(V)��ʱ��(t)�Ĺ�ϵ��ͼ����ʾ���ǿ��淴Ӧ2N02(g)
C(s)+H20(g)?��H>O��ѧ��Ӧ����(V)��ʱ��(t)�Ĺ�ϵ��ͼ����ʾ���ǿ��淴Ӧ2N02(g)  N204(g)?��H<O��Ũ��(c)��ʱ��(t)�ı仯���������˵������ȷ����??? (??? )
N204(g)?��H<O��Ũ��(c)��ʱ��(t)�ı仯���������˵������ȷ����??? (??? )
A��ͼһt2ʱ�ı�������������������¶Ȼ�������ѹǿ
B��ͼһt2ʱ�ı�������������˷�Ӧ���Ũ��
C��ͼ��t1ʱ�ı�������������������¶Ȼ�������ѹǿ
D����ͼ��t1ʱ�ı����������ѹǿ�����������ƽ����Է�����������С
�ο��𰸣�A
���������
���������A����ӦCO��g��+H2��g��?C��s��+H20��g����H��0������Ӧ�����������С���ȷ�Ӧ�������¶Ȼ�����ѹǿ���������ʶ�����ƽ��������Ӧ�����ƶ�������Ӧ����������࣬ͼһ��ʵ������ϣ���ȷ��B����Ӧ���ʱ�ֻ�ͷ�Ӧ���Լ�������������йأ�����C����Ӧ2NO2��g��?N2O4��g����H��0������Ӧ�����������С���ȷ�Ӧ������ѹǿ���ı������˲�䶼Ũ������ƽ��������Ӧ�����ƶ����������¶ȣ�ƽ�����淴Ӧ�����ƶ����ı�������˲�䣬Ũ�Ȳ��䣬ͼ����ʵ�ʲ����������D����ͼ��t1ʱ�̸ı��
�����Ѷȣ�һ��
3��ѡ���� ijһ��Ӧ���Ũ��Ϊ3mol/L,��5���Ӻ�,Ũ�ȱ�Ϊ2mol/L,����5����÷�Ӧ���ƽ����Ӧ������?????????????????????????????????????????????????????????��????????��
A��0.2 mol/s
B��0.2 mol��L/s
C��0.2 mol/��L��s��
D��12 mol/��L��min��
�ο��𰸣�CD
�����������
�����Ѷȣ���
4��ʵ���� ��10�֣�Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����������ͬѧ�ֱ��������ͼһ��ͼ����ʾ��ʵ�顣
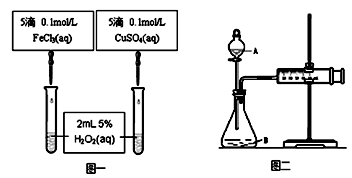
��1��ͼһ��ͨ���۲�_____________________________ ���������ԱȽϵó����ۡ���ͬѧ�����CuSO4��ΪCuCl2��Ϊ��������������__________________________��
����Ϊ���������������ָĽ��� _____________________________________________��
��2��ͼ�������ڶ����ȽϷ�Ӧ�Ŀ��������ͼ��װ�������Եķ����� ��
����ͼ����ʵ��ʱ������������� ��
�ο��𰸣���10�֣�(ÿ��2��)
��1����Ӧ�������ݿ�������Ӧ
���������(1���Ƚ����κ�ͭ�ζ�H2O2�ֽ�Ĵ�Ч�������ǹ۲�������ݵĿ���������ͭ���Ȼ�����������Ӳ�ͬ������Ӱ��ʵ�������ʽ�������Ӹij���ͬ�ģ������ų������ʵ������Ӱ�죬
��2����װ���л����ǻ�ģ���ͨ�����������������ı�װ���ڲ���ѹǿ��ǰ��ر�A��������
�÷�Ӧ��ͨ����������ķ�Ӧ���ʷ����жϵģ����Ը���v=��V/��t����֪����Ҫ�����������Dz���40ml��������Ҫ��ʱ��
�����Ѷȣ�һ��
5��ѡ���� ��Ӧ��X(g) + 3Y(g) 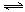 ?2Z(g) ;��H��0���ڲ�ͬ�¶�T����ͬѹǿ(P1>P2)�£��ﵽƽ��ʱ�����������Z�İٷֺ������¶ȱ仯������ӦΪ
?2Z(g) ;��H��0���ڲ�ͬ�¶�T����ͬѹǿ(P1>P2)�£��ﵽƽ��ʱ�����������Z�İٷֺ������¶ȱ仯������ӦΪ
�ο��𰸣�C
�����������
�����Ѷȣ���